See on neuromuskulaarse sünapsi vahendaja. Ained, mis blokeerivad ergastuse edasikandumist. Neuromuskulaarse sünapsi struktuur ja funktsioonid
Sünaps on spetsiaalne struktuur, mis tagab ergastuse ülekandumise ühelt ergastavalt struktuurilt teisele. Mõiste "synapse" võttis kasutusele C. Sherrington ja see tähendab "redutseerimist", "ühendust", "klambrit".
Sünapsi klassifikatsioon. Sünapsid võib klassifitseerida järgmiselt:
nende asukoht ja kuuluvus vastavatesse struktuuridesse:
* perifeerne (neuromuskulaarne, neurosekretoorne, retseptor-neuronaalne);
* tsentraalne (aksosomaatiline, aksodendriitne, aksoaksonaalne, somatodendriitne, somatosomaatiline);
nende tegevuse märk - ergastav ja inhibeeriv;
signaali edastamise meetod - keemiline, elektriline, segatud.
vahendaja, mille kaudu ülekanne toimub - kolinergiline, adrenergiline, serotonergiline, glütseriinergiline jne.
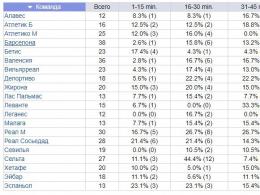
Sünapsi struktuur. Kõigil sünapsitel on palju ühist, seega võib sünapsi struktuuri ja selles sisalduva ergastuse ülekandemehhanismi käsitleda neuromuskulaarse sünapsi näitel (joonis 7).
Sünaps koosneb kolmest põhielemendist:
* presünaptiline membraan - (neuromuskulaarses sünapsis - see on paksenenud otsaplaat);
* postsünaptiline membraan;
* sünaptiline lõhe.
presünaptiline membraan- see on lihase membraani osa, mis lõpeb lihaskiuga kokkupuute piirkonnas. Postsünaptiline membraan on osa lihaskiudude membraanist. Postsünaptilise membraani osa, mis asub presünaptilise vastas, nimetatakse subsünaptiliseks membraaniks. Subsünaptilise membraani tunnuseks on spetsiaalsete retseptorite olemasolu selles, mis on teatud vahendaja suhtes tundlikud, ja kemosõltuvate kanalite olemasolu. Postsünaptilises membraanis, väljaspool subsünaptilist, on pingega seotud kanalid.
Ergastuse ülekandemehhanism keemilistes ergastavates sünapsides. Keemilise ülekandega sünapsides edastatakse erutus neurotransmitterite (vahendajate) abil. Valikud- need on kemikaalid, mis tagavad ergastuse edasikandumise sünapsides. Vahendajad jagunevad olenevalt nende olemusest mitmeks rühmaks:
* monoamiinid(atsetüülkoliin, dopamiin, norepinefriin, serotoniin jne);
* aminohapped (gamma-aminovõihape - GABA, glutamiinhape, glütsiin jne);
* neuropeptiidid(aine P, endorfiinid, neurotensiin, ACTH, angiotensiin, vasopressiin, somatostatiin jne).
Molekulaarses vormis vahendaja asub presünaptilise paksenemise (sünaptilise naastu) vesiikulites, kuhu see siseneb:
* neuroni perinukleaarsest piirkonnast kasutades kiiret aksonaalset transporti (aksovoolu);
* sünaptilistes otstes esineva mediaatori sünteesi tõttu selle lõhustumisproduktidest;
* neurotransmitteri tagasihaarde tõttu sünaptilisest pilust muutumatul kujul.
Kui erutus tuleb mööda aksonit selle otstesse, presünaptilisse membraan depolariseerub, millega kaasneb kaltsiumiioonide sisenemine rakuvälisest vedelikust närvilõpmesse. Sissetulevad kaltsiumiioonid aktiveerivad sünaptiliste vesiikulite liikumise presünaptilisele membraanile, nende kontakti ja nende membraanide hävitamise (lüüsi) koos vahendaja vabanemisega sünaptilisse pilusse. Selles difundeerub vahendaja subsünaptilisse membraani, millel asuvad selle retseptorid. Vahendaja koostoime retseptoritega viib peamiselt naatriumioonide kanalite avanemiseni. See viib subsünaptilise membraani depolariseerumiseni ja niinimetatud ergastava postsünaptilise potentsiaali (EPSP) tekkeni. Neuromuskulaarses ristmikul nimetatakse EPSP-d otsaplaadi potentsiaaliks (EPP). Depolariseeritud subsünaptilise membraani ja postsünaptilise membraani külgnevate osade vahel tekivad lokaalsed voolud, mis depolariseerivad membraani. Kui nad depolariseerivad membraani kriitilise tasemeni, tekib lihaskiu postsünaptilises membraanis aktsioonipotentsiaal, mis levib mööda lihaskiu membraane ja põhjustab selle kokkutõmbumise.
Keemiliselt inhibeerivad sünapsid. Need sünapsid on ergastuse ülekandemehhanismi poolest sarnased ergastava toime sünapsidega. Inhibeerivates sünapsides interakteerub vahendaja (näiteks glütsiin) subsünaptilise membraani retseptoritega ja avab selles kloriidikanalid, mis viib kloriidioonide liikumiseni piki kontsentratsioonigradienti rakku ja hüperpolarisatsiooni arengut subsünaptilisel membraanil. . On olemas niinimetatud inhibeeriv postsünaptiline potentsiaal (IPSP).
Varem arvati, et iga vahendaja vastab postsünaptilise raku spetsiifilisele reaktsioonile - ergastusele või inhibeerimisele ühel või teisel kujul. Nüüdseks on kindlaks tehtud, et üks vahendaja ei vasta kõige sagedamini mitte ühele, vaid mitmele erinevale retseptorile. Näiteks skeletilihaste neuromuskulaarsetes ühenduskohtades olev atsetüülkoliin toimib H-koliinergilistele retseptoritele (nikotiinitundlikud), mis avavad naatriumi (ja kaaliumi) jaoks laiad kanalid, mis tekitab EPSP (EPS). Vago-kardiaalsetes sünapsides toimib sama atsetüülkoliin M-kolinergilistel retseptoritel (muskariini suhtes tundlik), mis avavad selektiivsed kanalid kaaliumiioonide jaoks, seega tekib siin inhibeeriv postsünaptiline potentsiaal (IPSP). Järelikult määravad vahendaja toime ergastava või inhibeeriva olemuse subsünaptilise membraani omadused (täpsemalt retseptori tüüp), mitte vahendaja ise.
Keemiliste sünapside füsioloogilised omadused.
Ergastuse keemilise ülekandega sünapsitel on mitmeid ühiseid omadusi:
* Sünapside kaudu ergastamine toimub ainult ühes suunas (ühepoolselt). See on tingitud sünapsi struktuurist: vahendaja vabaneb ainult presünaptilisest paksenemisest ja interakteerub subsünaptilise membraani retseptoritega;
* ergastuse ülekanne sünapside kaudu on aeglasem kui närvikiu kaudu – sünaptiline viivitus;
* ergastuse ülekandmine toimub spetsiaalsete keemiliste vahendajate - vahendajate abil;
* sünapsides toimub ergastusrütmi transformatsioon;
* sünapsitel on madal labiilsus;
* sünapsid on väga väsinud;
* sünapsid on väga tundlikud keemiliste (sh farmakoloogiliste) ainete suhtes.
Ergutavad elektrilised sünapsid. Lisaks keemilise ergastuse ülekandega sünapsidele leidub elektrilise ülekandega sünapse valdavalt kesknärvisüsteemis (KNS). Ergastavaid elektrilisi sünapse iseloomustab väga kitsas sünaptiline lõhe ja külgnevate pre- ja postsünaptiliste membraanide väga madal takistus, mis tagab kohalike elektrivoolude tõhusa läbimise. Madal takistus on reeglina seotud mõlemat membraani läbivate põikkanalite olemasoluga, st rakust rakku liikumisega (vahekontakt). Kanalid moodustavad iga kontaktmembraani valgumolekulid (poolmolekulid), mis on ühendatud komplementaarselt. See struktuur on elektrivoolu jaoks kergesti läbitav.
Ergastuse ülekande skeem elektrilises sünapsis: presünaptilisest aktsioonipotentsiaalist põhjustatud vool ärritab postsünaptilist membraani, kus tekivad EPSP ja aktsioonipotentsiaal.
Põikkanalid ühendavad rakke mitte ainult elektriliselt, vaid ka keemiliselt, kuna need on läbitavad paljude madala molekulmassiga ühendite jaoks. Seetõttu moodustuvad reeglina sama tüüpi rakkude vahel (näiteks südamelihase rakkude vahel) põikkanalitega ergastavad elektrilised sünapsid.
Ergastavate elektriliste sünapside üldised omadused on järgmised:
* kiirus, (ületab oluliselt keemiliste sünapside oma);
* jälgiefektide nõrkus ergastuse ülekandmisel (selle tulemusena on järjestikuste signaalide liitmine neis praktiliselt võimatu);
* kõrge töökindlus – ergastuse ülekanne.
Ergutavad elektrilised sünapsid võivad tekkida soodsates tingimustes ja kaduda ebasoodsates tingimustes. Näiteks kui üks kontaktrakkudest on kahjustatud, elimineeritakse selle elektrilised sünapsid teiste rakkudega. Seda omadust nimetatakse plastilisuseks.
Elektrilised sünapsid võivad olla ühepoolsed või kahepoolsed.
Elektriliselt inhibeeriv sünaps. Koos ergastava toimega elektriliste sünapsidega võivad tekkida elektrilised inhibeerivad sünapsid. Sellise sünapsi näide on sünaps, mis moodustab kaladel Mauthneri neuroni väljundsegmendis närvilõpu. Inhibeeriv toime ilmneb presünaptilise membraani aktsioonipotentsiaali poolt põhjustatud voolu toimel. Presünaptiline potentsiaal põhjustab segmendi olulise hüperpolarisatsiooni ja hüperpolariseeriv vool pärsib koheselt aktsioonipotentsiaali teket aksoni algsegmendis.
AT segatud sünapsid presünaptiline aktsioonipotentsiaal tekitab tüüpilise keemilise sünapsi postsünaptilise membraani depolariseeriva voolu, kus pre- ja postsünaptiline membraan on üksteisega lõdvalt kõrvuti. Seega on nendes sünapsides keemiline ülekanne vajaliku tugevdava mehhanismina.
KESKNÄRVISÜSTEEMI FÜSIOLOOGIA.
KESKNÄRVISÜSTEEMI FUNKTSIOONID. Inimkeha on keerukas kõrgelt organiseeritud süsteem, mis koosneb funktsionaalselt omavahel seotud rakkudest, kudedest, elunditest ja nende süsteemidest.
Seda funktsioonide omavahelist seost (integratsiooni), nende koordineeritud toimimist tagab kesknärvisüsteem (KNS). Kesknärvisüsteem reguleerib kõiki kehas toimuvaid protsesse, mistõttu tema abiga toimuvad erinevate organite töös kõige adekvaatsemad muutused, mille eesmärk on tagada üks või teine tema tegevus.
Samuti suhtleb kesknärvisüsteem keha väliskeskkonnaga, analüüsides ja sünteesides retseptoritelt talle tulevat mitmesugust informatsiooni. See täidab teatud eksistentsitingimustes vajalikke käitumisregulaatori funktsioone. See tagab piisava kohanemise ümbritseva maailmaga. Lisaks on inimese vaimse tegevuse aluseks olevad protsessid seotud kesknärvisüsteemi funktsioonidega.
MEETODID KNS-i FUNKTSIOONIDE UURIMISEKS. Kesknärvisüsteemi funktsioonide intensiivne areng tõi kaasa ülemineku aju erinevate osade funktsioonide uurimise kirjeldavatelt meetoditelt eksperimentaalsetele meetoditele. Paljusid kesknärvisüsteemi funktsioonide uurimiseks kasutatavaid meetodeid kasutatakse üksteisega kombineeritult.
Kesknärvisüsteemi erinevate osakondade hävitamise (väljapressimise) meetod. Selle meetodi abil on võimalik kindlaks teha, millised kesknärvisüsteemi funktsioonid langevad pärast operatsiooni välja ja millised jäävad. Seda metoodilist tehnikat on eksperimentaalsetes füsioloogilistes uuringutes kasutatud pikka aega.
Transektsioonimeetod võimaldab uurida kesknärvisüsteemi teistest osakondadest tulevate mõjude olulisust ühe või teise kesknärvisüsteemi osakonna tegevuses. Transektsioon viiakse läbi kesknärvisüsteemi erinevatel tasanditel. Näiteks seljaaju või ajutüve täielik läbilõikamine eraldab kesknärvisüsteemi ülemised osad selle all olevatest osadest ja võimaldab uurida refleksreaktsioone, mida viivad läbi närvikeskused, mis asuvad närvikeskuse asukohast allpool. läbilõige. Üksikute närvikeskuste läbilõikamine ja lokaalne vigastus viiakse läbi mitte ainult katsetingimustes, vaid terapeutilise meetmena ka neurokirurgia kliinikus.
Ärrituse meetod võimaldab teil uurida kesknärvisüsteemi erinevate moodustiste funktsionaalset tähtsust. Teatud ajustruktuuride stimulatsiooniga (keemiline, elektriline, mehaaniline jne) saab jälgida ergastusprotsesside tekkimist, avaldumistunnuseid ja leviku olemust.
Elektroentsefalograafia on meetod aju erinevate osade elektrilise aktiivsuse registreerimiseks. Esimest korda registreeris aju elektrilise aktiivsuse VV Pravdich-Neminsky, kasutades ajju sukeldatud elektroode. Berger registreeris ajupotentsiaalid kolju pinnalt ja nimetas ajupotentsiaalide kõikumiste registreerimist elektroentsefalogrammiks (EEG-ma).
Võnkumiste sagedus ja amplituud võivad muutuda, kuid igal hetkel on EEG-s ülekaalus teatud rütmid, mida Berger nimetas alfa-, beeta-, teeta- ja deltarütmideks. Alfarütmi iseloomustab võnkesagedus 8-13 Hz, amplituud 50 μV. See rütm väljendub kõige paremini ajukoore kukla- ja parietaalpiirkondades ning registreeritakse füüsilise ja vaimse puhkuse tingimustes suletud silmadega. Kui silmad on avatud, asendub alfarütm kiirema beeta-rütmiga. Beetarütmi iseloomustab võnkesagedus 14-50 Hz ja amplituud kuni 25 μV. Mõnel inimesel puudub alfarütm ja seetõttu registreeritakse puhkeolekus beetarütm. Sellega seoses eristatakse beeta-rütmi 1 võnkesagedusega 16–20 Hz, see on iseloomulik puhkeolekule ja registreeritakse eesmises ja parietaalses piirkonnas. Beeta-rütm 2 sagedusega 20-50 Hz ja see on tüüpiline intensiivse ajutegevuse seisundile. Teeta rütm on võnkumine sagedusega 4-8 Hz ja amplituudiga 100-150 μV. See rütm registreeritakse ajalises ja parietaalses piirkonnas psühhomotoorse aktiivsuse ajal, stressi ajal, une ajal, hüpoksia ja kerge anesteesia ajal. Delta-rütmi iseloomustavad aeglased potentsiaalsed võnkumised sagedusega 0,5–3,5 Hz ja amplituudiga 250–300 μV. See rütm registreeritakse sügava une ajal, sügava anesteesia ajal, hüpoksia ajal.
EEG-meetodit kasutatakse kliinikus diagnostilistel eesmärkidel. See meetod on leidnud eriti laialdast rakendust neurokirurgia kliinikus ajukasvajate lokaliseerimise määramiseks. Neuroloogiakliinikus kasutatakse seda meetodit epilepsia fookuse lokaliseerimise määramiseks, psühhiaatriakliinikus - psüühikahäirete diagnoosimiseks. Kirurgilises kliinikus kasutatakse EEG-d anesteesia sügavuse kontrollimiseks.
Väljakutsutud potentsiaalide meetod on teatud ajustruktuuride elektrilise aktiivsuse registreerimine retseptorite, närvide ja subkortikaalsete struktuuride stimuleerimise ajal. Evokeeritud potentsiaalid (EP) esindavad kõige sagedamini EEG-we kolmefaasilisi võnkumisi, mis asendavad üksteist: positiivne, negatiivne, teine (hiljem) positiivne võnkumine. Need võivad aga olla ka keerulisemad. On olemas primaarsed (PO) ja hilised või sekundaarsed (VO) esilekutsutud potentsiaalid. EP on aju stimulatsiooni ajal registreeritud EEG fragment ja sellel on sama olemus kui elektroentsefalogrammil.
IP-meetod leiab rakendust neuroloogias ja neurofüsioloogias. EP abil saab jälgida aju juhtivusradade ontogeneetilist arengut, analüüsida sensoorsete funktsioonide esituse lokaliseerumist, analüüsida ajustruktuuride vahelisi seoseid, näidata lülitite arvu ergastuse levimise teel jne. .
Mikroelektroodi meetodil uuritakse üksiku neuroni füsioloogiat, selle bioelektrilist aktiivsust nii puhkeolekus kui ka erinevate mõjude all. Selleks kasutatakse spetsiaalselt valmistatud klaasist või metallist mikroelektroode, mille otsa läbimõõt on 0,5–1,0 µm või veidi rohkem. Klaasist mikroelektroodid on elektrolüüdilahusega täidetud mikropipetid. Sõltuvalt mikroelektroodi asukohast on rakkude bioelektrilise aktiivsuse ümbersuunamiseks kaks võimalust – rakusisene ja rakuväline.
Rakusisene salvestamine võimaldab registreerida ja mõõta:
* puhkemembraani potentsiaal;
* postsünaptilised potentsiaalid (EPSP ja TPSP);
* lokaalse ergastuse levikule ülemineku dünaamika;
* tegevuspotentsiaal ja selle komponendid.
Rakuväline määramine võimaldab registreerida:
* nii üksikute neuronite kui ka peamiselt nende elektroodi ümber paiknevate rühmade aktiivsus.
Erinevate ajustruktuuride asukoha täpseks määramiseks ja erinevate mikroobjektide (elektroodid, termopaarid, pipetid jne) sisestamiseks neisse on stereotaksiline meetod leidnud laialdast rakendust nii elektrofüsioloogilistes uuringutes kui ka neurokirurgia kliinikutes. Selle kasutamine põhineb üksikasjalike anatoomiliste uuringute tulemustel erinevate ajustruktuuride asukoha kohta kolju luuliste orientiiride suhtes. Selliste uuringute andmete põhjal on loodud spetsiaalsed stereotaksilised atlased nii erinevate loomaliikide kui ka inimeste jaoks. Praegu kasutatakse neurokirurgia kliinikus stereotaksia meetodit laialdaselt järgmistel eesmärkidel:
* ajustruktuuride hävitamine, et kõrvaldada hüperkineesi seisundid, alistamatu valu, mõned psüühikahäired, epilepsiahäired jne;
* patoloogiliste epileptogeensete koldete tuvastamine;
* radioaktiivsete ainete viimine ajukasvajatesse ja nende kasvajate hävitamine;
* ajuaneurüsmide koagulatsioon;
* terapeutilise elektrilise stimulatsiooni või ajustruktuuride pärssimise rakendamine.
KNS-I STRUKTUUR. Kesknärvisüsteemi struktuurne ja funktsionaalne üksus on neuron (närvirakk). See koosneb kehast (soma) ja protsessidest - arvukatest dendriitidest ja ühest aksonist. Dendriidid hargnevad tavaliselt tugevalt ja moodustavad koos teiste rakkudega palju sünapse, mis määrab nende juhtiva rolli info tajumisel neuroni poolt. Rakukehast saab alguse akson aksonikünkaga, mille ülesandeks on tekitada närviimpulss, mis kandub mööda aksonit teistesse rakkudesse. Akson hargneb tugevalt, moodustades palju kollateraale, mille otsad moodustavad sünapse teiste rakkudega. Sünapsi aksonmembraan sisaldab spetsiifilisi retseptoreid, mis võivad reageerida erinevatele vahendajatele või neuromodulaatoritele. Seetõttu saavad teised neuronid tõhusalt reguleerida neurotransmitterite vabanemise protsessi presünaptiliste lõppude kaudu. Lisaks sisaldab terminali membraan suurt hulka pingest sõltuvaid kaltsiumikanaleid, mille kaudu kaltsiumioonid sisenevad terminali, kui see on ergastatud.
Enamikus tsentraalsetes neuronites esineb AP aksoni künkliku membraani piirkonnas, mille erutusvõime on kaks korda kõrgem kui teistel piirkondadel, ja siit levib erutus mööda aksonit ja rakukeha. See neuroni ergastamise meetod on oluline selle integreeriva funktsiooni rakendamiseks, st võimeks kokku võtta mõjud, mis neuronile tulevad erinevate sünaptiliste radade kaudu. Neuroni erinevate osade erutuvuse aste ei ole sama, kõrgeim on see aksonikünka piirkonnas, neuroni kehapiirkonnas tunduvalt madalam, dendriitides kõige madalam.
Lisaks kesknärvisüsteemi neuronitele on gliiarakud, mis hõivavad poole aju mahust. Perifeerseid aksoneid ümbritseb ka gliiarakkude ümbris – Ivanovo rakud. Neuronid ja gliiarakud on eraldatud rakkudevaheliste lõhedega, mis suhtlevad üksteisega ja moodustavad vedelikuga täidetud neuronite ja gliia rakkudevahelise ruumi. Selle ruumi kaudu toimub ainete vahetus närvi- ja gliiarakkude vahel. Gliarakkude funktsioonid on mitmekesised:
* need on neuroneid toetav, kaitsev ja troofiline aparaat, säilitavad teatud kaaliumi- ja kaltsiumiioonide kontsentratsiooni rakkudevahelises ruumis;
* neelavad aktiivselt neurotransmittereid, piirates sellega nende aega
toimingud ja muud funktsioonid.
AXON TRANSPORT. Aksonid on lisaks ergastuse juhtimise funktsioonile kanalid erinevate ainete transpordiks. Rakukehas sünteesitud valgud ja vahendaja, organellid ja muud ained võivad liikuda mööda aksonit selle lõpuni. Seda ainete liikumist nimetatakse aksoni transpordiks. Seda on kahte tüüpi – kiire ja aeglane aksoni transport.
AKSONI KIIRE TRANSPORT on vesiikulite, mitokondrite ja mõningate valguosakeste transport rakukehast aksonilõppudesse (anterograadne transport) kiirusega 250-400 mm/ööpäevas. Seda teostab spetsiaalne transpordimehhanism - mikrotuubulite ja neurofilamentide abil ning sarnaneb lihaste kontraktsiooni mehhanismiga.
Kiire aksonite transport aksoni otstest rakukehasse ehk retrograadselt liigutab pinotsütoosi käigus aksonilõppudesse tekkivaid lüsosoome, vesiikuleid, näiteks atsetüülkoliinesteraasi, mõningaid viirusi, toksiine jne, kiirusega 220 mm/ööpäevas. Kiire anterograadse ja retrograadse transpordi kiirus ei sõltu aksoni tüübist ja läbimõõdust.
SLOW AXON TRANSPORT tagab liikumise kiirusega 1-4 mm/päevas. tsütoplasma valgud ja struktuurid (mikrotuubulid, neurofilamendid, RNA, transpordi- ja kanalimembraani valgud jne) distaalses suunas perikarüoni sünteetiliste protsesside intensiivsuse tõttu. Aeglane aksonite transport on eriti oluline neuroniprotsesside kasvu ja regenereerimise protsessides.
HELKORI TEOORIA ARENG.
Kesknärvisüsteemi tegevuse peamine mehhanism on refleks. Refleks on keha reaktsioon ärritaja tegevusele, mis viiakse läbi kesknärvisüsteemi osalusel ja mille eesmärk on saavutada kasulik tulemus.
Reflex tähendab ladina keeles "peegeldust" -. Esimest korda kasutas mõistet "peegeldus" või "peegeldamine" R. Descartes (1595-1650), et iseloomustada keha reaktsioone vastuseks meelte stimulatsioonile. Ta oli esimene, kes väitis, et kõik organismi efektortegevuse ilmingud on põhjustatud üsna reaalsetest füüsilistest teguritest. Pärast R. Descartes'i töötas refleksi idee välja Tšehhi teadlane G. Prochazka, kes töötas välja reflektiivsete toimingute doktriini. Sel ajal märgiti juba, et selgrooloomadel tekivad liigutused vastusena teatud nahapiirkondade ärritusele ja seljaaju hävimine viib nende kadumiseni.
Refleksiteooria edasiarendus on seotud I. M. Sechenovi nimega. Oma raamatus "Aju refleksid" väitis ta, et kõik teadvuseta ja teadliku elu teod on oma olemuselt refleksid. See oli geniaalne katse juurutada füsioloogiline analüüs vaimsetesse protsessidesse. Kuid sel ajal polnud ajutegevuse objektiivseks hindamiseks meetodeid, mis võiksid seda I. M. Sechenovi ettepanekut kinnitada. Sellise objektiivse meetodi töötas välja IP Pavlov - konditsioneeritud reflekside meetod, mille abil ta tõestas, et keha kõrgem närviaktiivsus, nagu ka madalam, on refleks.
Refleksi struktuurne alus, selle materiaalne substraat (morfoloogiline alus) on refleksikaar - morfoloogiliste struktuuride kogum, mis tagab refleksi rakendamise (tee, mida mööda erutus refleksi rakendamise ajal läbib).
Kaasaegse refleksitegevuse idee keskmes on kasuliku adaptiivse tulemuse kontseptsioon, mille nimel tehakse igasugune refleks. Info kasuliku adaptiivse tulemuse saavutamise kohta jõuab kesknärvisüsteemi tagasisidelingi kaudu pöördaferentatsiooni kujul, mis on refleksitegevuse kohustuslik komponent. Pöördaferentatsiooni põhimõtte tõi refleksiteooriasse P.K. Anokhin. Seega, tänapäevaste kontseptsioonide kohaselt ei ole refleksi struktuurne alus refleksi kaar, vaid refleksirõngas, mis koosneb järgmistest komponentidest (linkidest):
* retseptor;
* aferentne närvirada;
* närvikeskus;
* efferentne närvirada;
* töötav keha (efektor);
* vastupidine aferentatsioon (joon. 8).
Refleksi struktuurse aluse analüüs viiakse läbi refleksirõnga üksikute lülide (retseptor, aferentsed ja eferentsed rajad, närvikeskus) järjestikuse väljalülitamise teel. Kui refleksrõnga mis tahes lüli on välja lülitatud, kaob refleks. Järelikult on refleksi rakendamiseks vajalik selle morfoloogilise aluse kõigi lülide terviklikkus.
Kesknärvisüsteemi rakkudel on üksteisega arvukalt ühendusi, seega võib inimese närvisüsteemi kujutada närviahelate (närvivõrkude) süsteemina, mis edastavad ergastuse ja moodustavad inhibeerimise. Selles närvivõrgus võib erutus levida ühelt neuronilt paljudele teistele neuronitele. Ergastuse levimise protsessi ühelt neuronilt paljudele teistele neuronitele nimetatakse ergastuse või lahkneva printsiibi kiiritamine põnevuse levik.
Ergastuse kiiritamist on kahte tüüpi:
* suunatud ehk süsteemne kiiritamine, kui erutus levib läbi teatud neuronite süsteemi ja moodustab keha koordineeritud adaptiivse aktiivsuse;
* ebasüstemaatiline või hajus (mittesuunaline) kiiritamine, ergastuse kaootiline levik, mille korral koordineeritud tegevus on võimatu (joon. 9).
Kesknärvisüsteemis võivad erinevatest allikatest pärit ergastused koonduda ühte neuronisse. Seda ergastuste võimet koonduda samadele vahe- ja lõppneuronitele nimetatakse ergastuse konvergents(joonis 9).
Neuromuskulaarse sünapsi presünaptiline membraan on osa motoorse neuroni aksoni presünaptilise otsa membraanist, mis piirab sünaptilist lõhet. Selle kaudu vabaneb vahendaja (eksotoos) sünaptilisse pilusse. Presünaptilise lõpu vahendaja sisaldub 40 nm läbimõõduga sünaptilistes vesiikulites (vesiikulites). Need moodustuvad Golgi kompleksis, kiire otsese aksontranspordi abil toimetatakse presünaptilisse lõppu ning seal täidetakse need mediaatori ja ATP-ga. Neuromuskulaarses sünapsis on vahendajaks atsetüülkoliin, mis moodustub atsetüülkoensüümist A ja koliinist ensüümi koliinatsetüültransferaasi toimel. Vesiikulid paiknevad valdavalt presünaptilise membraani perioodiliste paksenemiste lähedal, mida nimetatakse aktiivseteks tsoonideks. Inaktiivses sünapsis on vesiikulid seotud tsütoskeleti valkudega sünapsiini valgu abil, mis tagab neile immobiliseerimise ja reserveerimise. Presünaptilise lõpu olulised struktuurid on mitokondrid, mis annavad energiat sünaptilise ülekande protsessi jaoks, siledad ER-paagid, mis sisaldavad ladestunud Ca iooni, mikrotuubulid ja mikrofilamendid, mis osalevad vesiikulite rakusiseses liikumises.
Neuromuskulaarse sünapsi sünaptilise lõhe laius on keskmiselt 50 nm. See sisaldab rakkudevahelist vedelikku ja mukopolüsahhariidide tihedat ainet ribade, sildade kujul, mida nimetatakse basaalmembraaniks ja mis sisaldab atsetüülkoliinesteraasi.
Postsünaptiline membraan sisaldab retseptoreid, mis on võimelised siduma neurotransmitteri molekule. Selle tunnuseks on väikeste voldikute olemasolu, mis moodustavad sünaptilisse pilusse avanevad taskud.
Seega on neuromuskulaarse sünapsi ergastuse ülekande peamised etapid:
1) motoorse neuroni ergastamine, aktsioonipotentsiaali levik presünaptilisele membraanile;
2) presünaptilise membraani kaltsiumioonide läbilaskvuse suurenemine, kaltsiumi vool rakku, kaltsiumi kontsentratsiooni suurenemine presünaptilises otsas;
3) sünaptiliste vesiikulite sulandumine presünaptilise membraaniga aktiivses tsoonis, eksotsütoos, vahendaja sisenemine sünaptilisse pilusse;
4) atsetüülkoliini difusioon postsünaptilisele membraanile, selle kinnitumine N-kolinergiliste retseptoritega, kemosõltuvate ioonkanalite avanemine;
5) valdav naatriumioonivool läbi kemosõltuvate kanalite, otsaplaadi läveülese potentsiaali teke;
6) aktsioonipotentsiaalide esinemine lihasmembraanil;
7) atsetüülkoliini ensümaatiline lõhustamine, lõhustumisproduktide tagastamine neuroni lõppu, mediaatori uute osade süntees.
Lihasrelaksandid on ravimid, mis vähendavad skeletilihaste toonust koos motoorse aktiivsuse vähenemisega kuni täieliku immobilisatsioonini.
Toimemehhanism - H-kolinergiliste retseptorite blokaad sünapsides peatab närviimpulsi tarnimise skeletilihastele ja lihased lõpetavad kokkutõmbumise. Lõõgastus käib alt üles, varbaotstest kuni näolihasteni. Diafragma lõdvestub viimasena. Juhtivus taastatakse vastupidises järjekorras.
Vastavalt retseptoritega suhtlemise tunnustele jagatakse lihasrelaksandid kahte rühma:
Depolariseerivad lihasrelaksandid - kokkupuutel retseptoritega põhjustavad nad sünapsi membraani püsivat depolarisatsiooni, millega kaasneb lihaskiudude lühiajaline kaootiline kokkutõmbumine (müofastsikulatsioonid), mis muutub lihaste lõõgastumiseks. Püsiva depolarisatsiooni korral neuromuskulaarne ülekanne peatub. Lihaste lõdvestumine on lühiajaline, tekib avatud membraanikanalite kinnipidamise ja repolarisatsiooni võimatuse tõttu. Metaboliseerub pseudokoliinesteraasi poolt, eritub neerude kaudu
Mittedepolariseerivad lihasrelaksandid – blokeerivad retseptoreid ja membraanikanaleid neid avamata, depolarisatsiooni põhjustamata
20. sajandil Silelihaste füsioloogilised omadused ja omadused
Lihaskoe peamised funktsioonid:
1. mootor – liikumise tagamine
2.staatiline - fikseerimise tagamine, sh teatud asendis
3. retseptor – lihastes on retseptorid, mis võimaldavad tajuda enda liigutusi
4.depositing – vesi ja osa toitaineid ladestuvad lihastesse.
Füsioloogilised omadused:
Kokkuleppelisus. Silelihase kontraktsiooni määrab ergastuse jaotuse eripära. Seoste ja nende elektriväljade kaudu interakteeruv rakurühm moodustab kimbu, mis on silelihaste struktuurne ja funktsionaalne üksus ning tõmbub kokku tervikuna Kontraktsiooni pikk kestus; Silelihaskiudude kontraktsiooniaeg on mitusada korda pikem kui põiki. Tänu sellele on silelihased kohanenud pikaajaliseks kokkutõmbumiseks ilma suurte energiakulutusteta ja väsivad aeglaselt;
Spontaanne müogeenne aktiivsus. Erinevalt skeletilihastest tekivad mao, soolte, emaka, kusejuhade, veresoonte ja teiste siseorganite silelihastel spontaansed teetaanilaadsed kokkutõmbed.See spontaanne tegevus toimub spetsiaalsetes lihasrakkudes, mis toimivad südamestimulaatorina, st neil on võime automatiseerida. Nendest rakkudest levib AP kiirusega umbes 0,1 m/s läbi Nexuse naaberkiududesse ja katab kogu lihase. Näiteks esinevad mao peristaltilised kokkutõmbed sagedusega 3 korda 1 minuti kohta, segmentaalsed ja pendli liikumised jämesooles - sagedusega -20 korda 1 minuti kohta.
Plastsus - võime säilitada venitades omandatud pikkust pinget muutmata. See omadus on väga oluline siseorganite, näiteks põie normaalseks toimimiseks.
kõrge tundlikkus füsioloogiliselt aktiivsete ainete, eriti autonoomse närvisüsteemi vahendajate - atsetüülkoliini, aga ka serotoniini, bradükiniini, prostaglandiinide suhtes. Need bioloogiliselt aktiivsed ained võivad nii silelihaskiude ergutada kui ka pärssida. Oleneb, milline protsess – depolarisatsioon või hüperpolarisatsioon põhjustab antud aine rakumembraanil. Näiteks atsetüülkoliin põhjustab enamiku elundite silelihaste kokkutõmbumist, kuid aitab mõne elundi veresoonte seinu lõdvestada. Silelihaste reaktsioonide olemus füsioloogiliselt aktiivse aine toimele sõltub sellest, kas see avab ioonikanaleid, mille omakorda määrab membraaniretseptorite spetsiifilisus.
Erutuvus. Puhkepotentsiaal 60-70 mV. Spontaanse elektrilise aktiivsusega müotsüütidele 30-60. AP positiivne tipp on väiksem kui vöötlihaskiududel, väiksem kui vöötlihaskiududel ja ulatub 10-15 mV-ni. AP kestus on vahemikus 25 ms kuni 1 s. Puhkepotentsiaali moodustumise protsessis ei mängi rolli mitte ainult K + ioonid, vaid ka Ca) Aktiini ja müosiini vastastikmõju silelihaskiududes aktiveerivad ka Ca 2 ioonid, kuid need ei sisene rakkudesse mitte sarko-retikulumist. , vaid transporditakse sinna rakkudevahelisest keskkonnast. Membraani depolarisatsiooni põhjustab kaltsiumikanalite avanemine ja kaltsiumiioonide difusioon rakku.
Juhtivus. Ergastuse juhtimine piki silelihase müotsüüti on pidev. Eraldi üksikud silelihasrakud aga ei erutu ega tõmbu kokku. Üksikute müotsüütide vaheline interaktsioon toimub madala elektritakistusega pilulaadsete kontaktide kaudu. Tänu sellele ergastab ühe raku elektriväli teist. AP levimiskiirus kiires on 5-10 m/s.
Automatiseerimine on omane südamestimulaatori rakkudele (stimulaatorid). See põhineb spontaanselt tekkival aeglasel depolarisatsioonil – kriitilise potentsiaali saavutamisel tekib AP. See depolarisatsioon on peamiselt tingitud kaltsiumiioonide difusioonist rakku.
2.Refleksi kaar- struktuuride komplekt, mille abil refleks viiakse läbi. Skemaatiliselt saab reflekskaare kujutada 5 lingilt.
1. Vastuvõttev lüli (retseptor) tagab keha välis- ja sisekeskkonna muutuste tajumise läbi ärritusenergia muundamise retseptori potentsiaaliks.
Refleksogeenne tsoon - retseptorite kogum, mille ärritus põhjustab refleksi. Igasuguse ärrituse korral tekivad retseptori potentsiaalid, mis tagavad n.i. kesknärvisüsteemis 2 lüli abil.
2. Aferentne link
Roll: signaali edastamine kesknärvisüsteemis reflekskaare kolmandale lülile. Somaatilise närvisüsteemi jaoks on see aferentne neuron koos oma protsessidega, selle keha asub seljaaju ganglionides või kraniaalnärvide ganglionides. Impulss mööda aferentse neuroni dendriiti, seejärel mööda selle aksonit, seejärel kesknärvisüsteemi.
3. Juhtlüli on tsentraalsete (ANS-i ja PNS-i jaoks) neuronite kogum, mis moodustavad keha vastuse.
4. Eferentne lüli on efektorneuroni (somaatilise NS motoorse neuroni jaoks) akson.
5. Somaatilise n.s. efektor (tööorgan) efektorneuron. on motoorne neuron
Reflekside klassifikatsioon
1. Vastavalt reflekside ilmnemise tingimustele ontogeneesis
a) kaasasündinud (tingimusteta)
b) Omandatud
Kaasasündinud võib olla somaatiline (somaatilise. n.s. abiga, efektorina - skeletilihased) ja vegetatiivne (veget. n.s. abiga)
2. Bioloogilise tähtsuse järgi
a) Homeastaatiline (siseorganite funktsioonide reguleerimine; südame töö; seedetrakti sekretsioon ja motoorika - toidurefleksid.)
b) kaitsev (kaitsev)
c) Seksuaalne
d) orienteeruv refleks.
3. Olenevalt sünapside arvust
Keskosas eristatakse reflekskaaret.
a) monosünaptiline (refleks nelipealihase venitamiseks - põlve sirutajarefleks kõõluse löömisel
b) polüsünaptiline (osaleb mitu järjestikku ühendatud kesknärvisüsteemi neuronit).
4. retseptorite poolt, mille ärritus põhjustab reaktsiooni.
a) eksterotseptiivne
b) interotseptiivne
c) propriotseptiivne (kasutatakse kliinilises praktikas kesknärvisüsteemi erutuvuse seisundi hindamiseks ja diagnoosimiseks).
5. reflekskaare lokaliseerimisega
A) keskne (kaar läbi kesknärvisüsteemi)
b) perifeersed refleksid (kaar sulgub väljaspool kesknärvisüsteemi)
c) seoses füsioloogiliste süsteemidega
|
MÄRGID |
VEGETATIIVNE |
SOMAATIKA |
|
sihtorganid |
Silelihased, müokard, näärmed, rasvkude, immuunorganid |
Skeletilihased |
|
Paravertebraalne, prevertebraalne ja organ |
Lokaliseeritud kesknärvisüsteemis |
|
|
Efferentsete neuronite arv | ||
|
Stimuleeriv toime |
Erutav või supresseeriv |
Põnev |
|
Närvikiudude tüübid |
Õhuke müeliniseerunud või mittemüeliniseerunud, aeglane |
müeliini kiire |
Sünaps(gr. sünapsis- ühendus) on spetsiaalne struktuur, mis tagab signaali edastamise elemendist rakku. Sünapsi kaudu realiseeritakse paljude farmakoloogiliste ravimite toime.
Struktuur-funktsionaalne korraldus. Igal sünapsil on eel- ja postsünaptiline membraan ja sünaptiline lõhe(joonis 17).
Riis. 17. Skeletilihase neuromuskulaarne sünaps: 1 - aksoni haru; 2 - aksoni presünaptiline lõpp; 3 - mitokondrid; 4 - atsetüülkoliini sisaldavad sünaptilised vesiikulid; 5 - sünaptiline lõhe; 6 - vahendaja molekulid sünaptilises pilus; 7 - N-kolinergiliste retseptoritega lihaskiu postsünaptiline membraan
presünaptiline membraan Neuromuskulaarne sünaps on osa motoorse neuroni aksoni presünaptilise otsa membraanist. See vabastab (eksotsütoos) vahendaja(lat. vahendaja vahendaja) sünaptilisse pilusse. Neuromuskulaarses sünapsis on vahendajaks atsetüülkoliin. Presünaptilise lõpu vahendaja sisaldub sünaptilistes vesiikulites (vesiikulites), mille läbimõõt on umbes 40 nm. Need moodustuvad Golgi kompleksis, kiire aksontranspordi abil viiakse presünaptilisse lõppu, kus täidetakse vahendaja ja ATP-ga. Presünaptiline terminal sisaldab mitu tuhat vesiikulit, millest igaüks sisaldab 1000 kuni 10 000 keemilist molekuli.
postsünaptiline membraan (otsaplaat neuromuskulaarses sünapsis) on innerveeritud lihasraku rakumembraani osa, mis sisaldab retseptoreid, mis on võimelised siduma atsetüülkoliini molekule. Selle membraani eripära: palju väikseid voldid, mis suurendavad selle pindala ja sellel olevate retseptorite arvu 10-20 miljonini ühes sünapsis.
sünaptiline lõhe neuromuskulaarses sünapsis on keskmine laius 50 nm. See sisaldab rakkudevahelist vedelikku, atsetüülkoliinesteraasi ja mukopolüsahhariidide tihedat ainet ribade, sildade kujul, mis koos moodustavad alusmembraani, mis ühendab pre- ja postsünaptilisi membraane.
Sünaptilise ülekande mehhanismid sisaldama kolm major etapp(joonis 18).
Riis. 18. Impulsi juhtimise mehhanism läbi keemilise sünapsi: 1-8 - protsessi etapid (Chesnokova, 2007)
Esimene aste- vahendaja vabastamise protsess sünaptilisse lõhe, mille käivitab presünaptilise lõpu AP. Selle membraani depolarisatsioon viib pingega seotud Ca-kanalite avanemiseni. Ca 2+ siseneb närvilõpmesse vastavalt elektrokeemilisele gradiendile. Osa presünaptilises otsas olevast mediaatorist paikneb seestpoolt presünaptilisel membraanil. Ca 2+ aktiveerib presünapsi eksotsütootilise aparatuuri, mis kujutab endast presünaptilise lõpu valkude kogumit (sünapsiin, spektriin jne), mille aktiveerumine tagab atsetüülkoliini vabanemise eksotsütoosi kaudu sünaptilisse pilusse. Presünaptilisest otsast vabaneva atsetüülkoliini kogus on võrdeline neljanda astmega sinna sisenenud Ca 2+ kogusele. Ühe AP puhul väljutatakse neuromuskulaarse sünapsi presünaptilisest otsast 200-300 vahendajat (vesiikulit).
Teine faas - atsetüülkoliini difusioon 0,1-0,2 ms jooksul postsünaptilise membraanini ja selle mõju N-kolinergilistele retseptoritele (stimuleerib ka nikotiin, mistõttu nad said oma nime). Atsetüülkoliini eemaldamine sünaptilisest lõhest toimub selle hävitamisega atsetüülkoliinesteraasi toimel, mis asub sünaptilise lõhe basaalmembraanis, mõne kümnendiku millisekundi jooksul. Umbes 60% koliinist võtab presünaptiline lõpp tagasi, mis muudab vahendaja sünteesi säästlikumaks, osa atsetüülkoliinist hajub . AP-de vahelistes intervallides toimub presünaptilisest lõpust 1 s jooksul spontaanne 1–2 saatjakvanti vabanemine sünaptilisse lõhe, moodustades nn. miniatuursed potentsiaalid(0,4-0,8 mV). Nad säilitavad innerveeritud raku kõrge erutatavuse funktsionaalse puhkeoleku tingimustes ja täidavad troofilist rolli ning aitavad kesknärvisüsteemis säilitada selle keskuste toonust.
Kolmas etapp - atsetüülkoliini interaktsioon postsünaptilise membraani N-kolinergiliste retseptoritega, mille tulemusena avanevad ioonikanalid 1 ms ja N + rakku sisenemise ülekaalu tõttu toimub postsünaptilise membraani (otsaplaadi) depolarisatsioon. Seda neuromuskulaarse ristmiku depolarisatsiooni nimetatakse otsaplaadi potentsiaal(PKP) (joonis 19).
Skeletilihaskiu neuromuskulaarse sünapsi tunnuseks on see, et selle ühekordsel aktiveerimisel moodustub suure amplituudiga PKP (30-40 mV), mille elektriväli põhjustab AP tekke lihaskiu membraanil lihaskiudude lähedal. sünaps. PKP suur amplituud on tingitud asjaolust, et närvilõpmed on jagatud arvukateks harudeks, millest igaüks viskab välja neurotransmitteri.

Riis. 19. Otsaplaadi potentsiaal (Schmidt, 1985): KP– kriitiline potentsiaal; PD - tegevuspotentsiaal; AGA- PKP normaalses lihases; B- kurariseeritud lihase nõrgenenud PKP; nooled stiimuli rakendamise hetk
Ergastuse juhtivuse tunnused keemilistes sünapsides. Ergastuse ühepoolne juhtimine närvikiust närvi- või efektorrakku, kuna presünaptiline ots on tundlik ainult närviimpulsi suhtes ja postsünaptiline membraan on tundlik vahendaja suhtes.
Isoleerimata- külgnevate postsünaptiliste membraanide ergastus on kokku võetud.
sünaptiline viivitus signaali edastamisel teise rakku (neuromuskulaarses sünapsis 0,5-1,0 ms), mis on seotud vahendaja vabanemisega närvilõpmest, selle difusiooniga postsünaptilisse membraani ja postsünaptiliste potentsiaalide tekkega, mis võivad põhjustada AP-d.
Vähendamine (summutus) ergastus keemilistes sünapsides koos vahendaja ebapiisava vabanemisega presünaptilistest lõppudest sünaptilistesse lõhedesse.
Madal labiilsus(neuromuskulaarses sünapsis on 100 Hz), mis on 4-8 korda madalam kui närvikiu labiilsus. See on tingitud sünaptilisest viivitusest.
Neuromuskulaarse sünapsi (nagu ka kesknärvisüsteemi keemiliste sünapside) juhtivus on pärsitud või vastupidi, stimuleerivad erinevad ained.
Näiteks kurare ja curare-laadsed ained (diplatsiin, tubokurariin) seonduvad pöörduvalt postsünaptilise membraani N-kolinergiliste retseptoritega, blokeerides atsetüülkoliini toimet sellele ja edasikandumist sünapsis. Vastupidi, mõned farmakoloogilised ravimid, nagu proseriin, inhibeerivad atsetüülkoliinesteraasi aktiivsust, aidates kaasa atsetüülkoliini mõõdukale akumulatsioonile ja hõlbustades sünaptilist ülekannet, mida kasutatakse meditsiinipraktikas.
Väsimus(sünaptiline depressioon) - juhtivuse halvenemine kuni ergastuse juhtivuse täieliku blokeerimiseni koos sünapsi pikaajalise toimimisega (peamine põhjus - neurotransmitterite ammendumine presünaptilises terminalis).
Küsimused enesekontrolliks
1. Milline on ergastuse levimise mehhanism piki närvikiudu? Milline on Ranvieri sõlmede roll ergastuse juhtimisel mööda müeliniseerunud närvikiudu?
2. Mis on ergastuse spasmilise (soolava) leviku eelis selle pideva juhtivuse ees piki kiudmembraani?
3. Mis on närvikiudude isoleeritud ergastuse juhtivuse füsioloogiline tähtsus?
4. Millised närvikiud (aferentsed või eferentsed, vegetatiivsed või somaatilised) kuuluvad A-rühma? Kui suur on nende kaudu ergastamise kiirus?
5. Millised närvikiud (aferentsed või eferentsed, vegetatiivsed või somaatilised) kuuluvad B rühma? Kui suur on nende ülejuhtimise kiirus?
6. Millised närvikiud (aferentsed või eferentsed, vegetatiivsed või somaatilised) kuuluvad rühma C? Kui suur on nende kaudu ergastamise kiirus?
7. Loetlege neuromuskulaarse sünapsi (skeletilihase) struktuurid. Mis on otsaplaat?
8. Loetlege protsesside jada, mis viivad mediaatori vabanemiseni presünaptilisest membraanist sünapsilõhesse ergastuse edastamise ajal sünapsis.
9. Kas otsaplaadi potentsiaal on lokaalne potentsiaal või leviv ergutus?
10. Millised on otsaplaadi miniatuursed potentsiaalid, milline on nende tekkimise mehhanism?
11. Milline on närvi troofiline toime neuromuskulaarse sünapsi kaudu lihasele?
12. Millised ained on vahendajad sile- ja vöötlihaste neuromuskulaarsetes sünapsides?
13. Mis on sensoorne retseptor?
14. Millisesse kahte rühma jagunevad sensoorsed retseptorid kohanemiskiiruse järgi? Nimetage igaühega seotud retseptorid.
15. Mida mõeldakse primaarsete ja sekundaarsete retseptorite all?
16. Loetlege retseptorite peamised omadused.
17. Mida nimetatakse retseptori kohanemiseks? Kuidas muutub impulsside sagedus aferentses närvikius retseptori adaptatsiooni käigus?
18. Nimetage primaarsete ja sekundaarsete retseptorite ergastamisel tekkivad lokaalsed potentsiaalid.
19. Retseptoripotentsiaal, kus see tekib, mis on selle tähtsus?
20. Generaatori potentsiaal, kust see tekib, mis on selle tähtsus?
21. Kus tekib aktsioonipotentsiaal, kui esmane sensoorne retseptor on ergastatud?
22. Kus tekib aktsioonipotentsiaal sekundaarse sensoorse retseptori ergastamisel?
Lihaste füsioloogia
1.3.1. Skeletilihaste struktuursed ja funktsionaalsed omadused
lihaseid alajaotatud triibuline (skeleti ja südame) ja sile(veresooned ja siseorganid, välja arvatud süda).
Skeletilihas sisaldab lihaskiud, mis on struktuurselt ja funktsionaalselt üksteisest eraldatud, mis on piklikud mitmetuumalised rakud. Kiu paksus on 10-100 mikronit ja selle pikkus varieerub mõnest millimeetrist mitme sentimeetrini. Lihaskiudude arv, mis on muutunud konstantseks 4-5-ndal postnataalse ontogeneesi kuul, ei muutu hiljem; vanusega muutuvad (suurenevad) ainult nende pikkus ja läbimõõt.
Peamiste konstruktsioonielementide määramine. Lihaskiu põhielementide omadused. Lihaskiu rakumembraanist (sarcolemma) ulatuvad arvukad põikisuunalised invaginatsioonid sügavale ( T-tuubulid), mis tagavad selle koostoime sarkoplasmaatilise retikulumiga ( SPR) (joonis 20).

Riis. Joonis 20. Sarkoplasmaatilise retikulumi rakumembraani (1), põiktuubulite (2), külgmiste tsisternide (3) ja pikisuunaliste tuubulite (4), kontraktiilsete valkude (5) omavaheline seos: A - puhkeasendis; B - lihaskiudude kokkutõmbumise ajal; täpid tähistavad Ca 2+ ioone
SPR on omavahel ühendatud paakide ja nendest pikisuunas ulatuvate tuubulite süsteem, mis paiknevad müofibrillide vahel. SPR terminali (terminal) tsisternid külgnevad T-tuubulitega, moodustades nn. kolmkõlad. Mahutid sisaldavad Ca 2+, mis mängib olulist rolli lihaste kokkutõmbumisel. Sarkoplasma sisaldab rakusiseseid elemente : tuumad, mitokondrid, valgud (sh müoglobiin), rasvatilgad, glükogeenigraanulid, fosfaate sisaldavad ained, erinevad väikesed molekulid ja elektrolüüdid.
müoibrillid- lihaskiudude subühikud. Ühes lihaskius võib olla rohkem kui 2 tuhat müofibrill, nende läbimõõt on 1-2 mikronit. Üks müofibrill sisaldab 2-2,5 tuhat mikrofilamenti. protofibrillid- paralleelsed valguahelad ( õhuke - aktiin, paks - müosiin). Aktiinfilamendid koosnevad kahest spiraalis keerdunud alaühikust. Õhukeste filamentide koostis sisaldab ka reguleerivaid valke - tropomüosiin ja troponiin(joonis 21).
Riis. 21. Müofibrillide struktuurielementide vastastikune paigutus nende lõõgastumise (A, B) ja kokkutõmbumise (C) ajal
Need ergastamata lihases olevad valgud häirivad aktiini ja müosiini vastastikust suhet, mistõttu on puhkeolekus lihased lõdvestunud. Müofibrillid hõlmavad järjestikku ühendatud plokke - sarkomeerid(B) üksteisest eraldatud muud Z-triibud. Sarkomeer (pikkus 2-3 µm) on lihaskiudude kontraktiilne üksus; pikkusega 5 cm, see sisaldab umbes 20 tuhat järjestikku ühendatud sarkomeeri. Üksiku lihaskiu müofibrillid on omavahel ühendatud nii, et sarkomeeride asukoht langeb kokku ja see loob valgusmikroskoobis vaadeldes pildi kiu põikitriibutusest (joonis 22).
Riis. 22. Skeletilihase müotsüütide sarkomeer (A. Vander, J. Sherman, D. Luciano, 2004)
Sarkomeeri elemendid(vt joonis 21). Müosiini protofibrillid moodustavad sarkomeeri tumedaima osa - A-ketas(anisotroopne, polariseerib tugevalt valget valgust). A-ketta keskel asuvat heledamat ala nimetatakse H-tsoon. Kahe A-ketta vahelist sarkomeeri valgusala nimetatakse 1-ketas(isotroopne, peaaegu ei polariseeri valgust). Selle moodustavad Z-ribadest mõlemas suunas kulgevad aktiini protofibrillid. Igal sarkomeeril on kaks komplekti õhukesi filamente, mis on kinnitatud Z-ribade külge, ja üks komplekt jämedaid filamente, mis on tsentreeritud A-kettale. Lõdvestunud lihases kattuvad paksude ja õhukeste filamentide otsad A- ja 1-ketta piiril erineval määral üksteisega.
Lihaskiudude klassifikatsioon:
Struktuursete ja funktsionaalsete omaduste järgi ja värv eristavad kahte peamist lihaskiudude rühma: kiire ja aeglane.
Valge (kiire) lihaskiud sisaldavad rohkem müofibrillid ja vähem - mitokondreid, müoglobiini ja rasvu, kuid rohkem glükogeeni ja glükolüütilisi ensüüme; neid kiude nimetatakse glükolüütiline. Neid kiude ümbritsev kapillaarvõrk on suhteliselt hõre. Nende kiudude töötsükli kiirus on umbes 4 korda suurem kui aeglastel, mis on seletatav kiirete kiudude suurema ATPaasi aktiivsusega, kuid neil on madal vastupidavus. Valgetes lihaskiududes on aktiini ja müosiini filamente rohkem kui punastes, seetõttu on need paksemad ja nende kokkutõmbumisjõud suurem kui punastes kiududes.
Punased lihaskiud sisaldavad palju mitokondreid müoglobiin, rasvhapped. Neid kiude ümbritseb tihe verekapillaaride võrgustik ja nende läbimõõt on väiksem. Mitokondrid tagavad kõrge oksüdatiivse fosforüülimise taseme, mistõttu neid kiude nimetatakse oksüdatiivne. Punased lihaskiud on jaotatud kahte alarühma: kiire ja aeglane. Aeglased kiud võivad teha tööd suhteliselt pikka aega; väsimus areneb neil aeglasemalt. Nad on rohkem kohandatud tooniliste kontraktsioonidega. Punane kiiresti Väsimuse osas asuvad kiud valgete ja punaste aeglaste kiudude vahel. Nende kokkutõmbumise kiirus on lähedane valgete kiudude kokkutõmbumiskiirusele, mis on samuti seletatav müosiini kõrge ATPaasi aktiivsusega punastes kiiretes kiududes.
Samuti on väike hulk tõelisi toniseerivaid lihaskiude; neid lokaliseerivad 7-10 sünapsi, mis reeglina kuuluvad mitmesse motoorset neuronit, näiteks okulomotoorsetes lihastes, keskkõrva lihastes. Nende lihaskiudude PKP ei põhjusta neis AP teket, vaid vallandab otseselt lihaste kontraktsiooni.
lihaskiudude rühm motoorne (neuromotoorne) üksus. Kiireid ja täpseid liigutusi sooritavates lihastes, näiteks okulomotoorses, koosnevad neuromotoorsed üksused 3-5 lihaskiust. Lihastes, mis sooritavad vähem täpseid liigutusi (näiteks kehatüve ja jäsemete lihased), hõlmavad motoorsed üksused sadu ja tuhandeid lihaskiude. Suur motoorne üksus, võrreldes väikesega, sisaldab suhteliselt paksu aksoniga suurt motoorset neuronit, mis moodustab lihases suure hulga terminaalseid harusid ja innerveerib seetõttu suurt hulka lihaskiude. Kõik ühe motoorse üksuse lihaskiud, olenemata nende arvust, on sama tüüpi. Kõik skeletilihased on oma koostiselt segunenud, st. koosneb punastest ja valgetest lihaskiududest.
Kõigi lihaste spetsiifiline omadus on kontraktiilsus– kokkutõmbumisvõime, s.o. lühendada või arendada pingeid. Selle võime rakendamine toimub ergastuse ja selle juhtimise abil piki lihaskiudu. (vastavalt erutuvuse ja juhtivuse omadused).
Skeletilihastel puudub automaatsus, neid juhib keha meelevaldselt kesknärvisüsteemist tulevate impulsside abil, seetõttu nimetatakse neid ka nn. meelevaldne. Silelihased ei tõmbu ise kokku, seega nimetatakse neid ka tahtmatu aga neil on automatiseerimine.
Skeletilihaste funktsioonid:
Keha füüsilise aktiivsuse tagamine- vee ja toidu otsimine ja hankimine, selle püüdmine, närimine, neelamine, kaitsereaktsioonid, töötegevus - kunstniku, kirjaniku, teadlase, helilooja füüsiline ja loominguline töö väljendub lõpuks liikumises: joonistamises, kirjutamises, pillimängus jne P.
Hingamise tagamine(rindkere ja diafragma liigutused).
Kommunikatiivne funktsioon(suuline ja kirjalik kõne, näoilmed ja žestid).
Osalemine protsessides termoregulatsioon organism, muutes kontraktiilse termogeneesi intensiivsust.
©2015-2019 sait
Kõik õigused kuuluvad nende autoritele. See sait ei pretendeeri autorlusele, kuid pakub tasuta kasutamist.
Lehe loomise kuupäev: 2016-04-15
Närvikiud ei puutu otseselt lihaskiuga kokku. Nende vahel on väga kitsas vahe (20–50 nm). Närvilõp, lihaskiu osa, millega see ots külgneb, ja nendevaheline vahe moodustavad neuromuskulaarse sünapsi. Närvikiud lõpeb sünaptilise naastuga, mis sisaldab Mtokondreid ja märkimisväärsel hulgal (umbes 300 tuhat) vesiikuleid, kuhu on koondunud vahendaja – aine, millega erutus levib närvist lihasesse. Neuromuskulaarses ristmikus on selleks vahendajaks atsetüülkoliin. Atsetüülkoliini süntees toimub sünaptilises naastudes ja nõuab energiakulu. Vahega külgnevat naastu osa nimetatakse presünaptiliseks membraaniks. Lõhe teisel poolel on postsünaptiline membraan, mis kuulub lihaskiudude hulka. Selle membraani osa, mis on vahetult naastu kõrval, nimetatakse terminali kihiks.
Postsünaptilise membraani koostis sisaldab retseptorvalke (molekulmass - umbes 275 000), mis reageerivad atsetüülkoliinile ja mida nimetatakse kolinergilisteks retseptoriteks. Nad reageerivad ka nikotiinile, sellest ka nende nimi - H-kolinergilised retseptorid. Atsetüülkoliini reaktsioon H-kolinergiliste retseptoritega põhjustab retseptori molekulis konformatsioonilisi muutusi. See mõjutab lähedal asuvat kemosensitiivset ioonikanalit, mis võib läbida Na +, K +, Ca2 +. Nende kanalite valgustruktuurid on negatiivse laenguga ja seetõttu anioonid neid ei läbi.
Teabe edastamine neuromuskulaarse sünapsi kaudu toimub järgmises järjestuses:
1. PD tuleb naastudele närvikiudude kaudu.
2. AP toimel närvilõpme membraanile avanevad Ca2+ kanalid ja need ioonid sisenevad naastu.
3. Ca2 + kontsentratsiooni suurenemine naastudes viib (kalmoduliini osalusel) vahendaja vabanemiseni vesiikulitest sünaptilisse pilusse. Ühe AP toime tõttu väljub neurotransmitter ligikaudu 300 vesiikulist.
4. Atsetüülkoliin hajub läbi pilu.
5. Atsetüülkoliin reageerib H-kolinergiliste retseptoritega.
6. Kemosensitiivsete kanalite "väravad" avanevad ja kontsentratsioonigradiendi taga läheb Na + lihaskiudu ja K + - välja.
7. Toimub otsaplaadi depolariseerumine ja areneb selle potentsiaal (PKP). PEP on üks lokaalse ergastuse liike. Mida rohkem atsetüülkoliini vabaneb, seda rohkem väljendub see potentsiaal.
8. Kui LTL saavutab kriitilise väärtuse (CEC), kolossünaptiline elektrostimuleeriv membraan depolariseerub ja areneb.
AP lihaskiust, mis ulatub sünapsi mõlemale poole. Sellesse protsessi on kaasatud potentsiaaliga piiratud ioonikanalid.
Atsetüülkoliin vabaneb väikestes kogustes isegi siis, kui PD-d ei varustata närvikiududega. Isegi sellises koguses (transmitteri kvantid) põhjustab see postsünaptilise membraani kerge depolarisatsiooni (mV fraktsioonid), mida nimetatakse miniatuurseteks otsplaadipotentsiaalideks (MEPP).
Sünaptilisse pilusse vabanev atsetüülkoliin hävitatakse väga kiiresti ensüümi atsetüülkoliinesteraasi toimel. Selle tulemusena moodustub koliin, mis siseneb sünaptilisse naastu ja osaleb uute atsetüülkoliini osade loomises.
Info edastamine neuromuskulaarses sünapsis toimub ühes suunas, teatud viivitusega (umbes 0,5 ms). Liiga sagedaste ja pikaajaliste ärrituste korral võivad tekkida atsetüülkoliini reservide ammendumine ja väsimus; meetodid on neuromuskulaarsete sünapside impulsside mitteedastusvõime tugevdamise või nõrgendamise meetodid. Seega saab neid parandada atsetüülkoliin-kolinomimeetikumide (näiteks karbakooli) või atsetüülkoliinesteraasi (ezeriini, füsostigmiini) inaktiveerimisega. Sel juhul vahendajat ei hävitata, tema tegevust tõhustatakse ja pikeneb.
Ülekannet on võimalik nõrgestada või peatada kurare-laadsete ainete – lihasrelaksantide (näiteks tubokurariin, diplatsiin) – sisseviimisega. Need ravimid seonduvad kolinergiliste retseptoritega ja blokeerivad atsetüülkoliini toimet.
Närvide füsioloogia.
Inimese kesknärvisüsteem koosneb närvirakkudest, millest igaühel on üks akson ja palju dendriite. Närvikiud jagunevad: lihavad ja mittelihalised. Kõigil neil on Schwanni ümbris ja lihavad on lisaks kaetud ka müeliinkestaga, mille vahel on Ranvieri sõlmed, milles müeliinkesta puudub. Mittelihakad kiud on väikese läbimõõduga, alla 1,3 mikroni, väikese impulsi levimiskiirusega kuni 2 m/s ja PD kestusega 2 ms. Lihakad tekkisid mittelihalistest, läbimõõt kuni 25 mikronit, ergastuse levimise kiirus kuni 120 m/sek, AP kestus 0,4-0,5 msek.
AP jaotus piki mittelihavat kiudu: Saksa füsioloog Hermann pakkus välja "lokaalsete voolude" teooria, mille kohaselt ergastuse levimisel närvikiu membraanile ergastatud ja ergastamata ala vahel tekib lokaalne vool, mis on ergastamata piirkonna jaoks ärritaja. Kui selle väärtus on piisav PD esinemiseks naaberlõigus, siis PD laieneb sellele alale.
Kohalike voolude jaotus mittemessiilsetes närvikiududes on otseselt võrdeline membraani takistusega ja pöördvõrdeline rakusisese ja rakuvälise keskkonna takistusega. Vahemaa, mille kaudu kohalikud voolud levivad, on seda suurem, seda suurem on PD amplituud ja seda madalam on lävipotentsiaal.
Viljalistes kiududes tekib erutus, kui ärritus rakendatakse Ranvieri sõlmedes (Tasaki teooria) ja levib piki kiumembraani soolases (hüppelaadses) viisil (joonis 1).
Joonis 1. Ergastuse juhtimine mööda müeliniseerunud närvikiudu.
Sel juhul võib see katta mitte ainult ühte, vaid ka kahte Ranvieri lõikepunkti, mis tagab töökindluse ning suurendab ka ergastuse levimise kiirust ja on majanduslikult kasulikum, kuna energiat kulub mitte ühe impulsi kohta 20 korda rohkem. -lihakas kiudaine kui viljalihas. Seega on kiirus ja vahemaa, mille jooksul ergastus mittemedullaarsetes kiududes levib, võrdeline läbimõõdu, membraani takistuse ja AP amplituudiga; paberimassis on otseselt võrdeline vahepiirkondade pikkusega ja nende pikkus on seda suurem, mida suurem on kiu läbimõõt. Kiirus ei sõltu stimulatsiooni tugevusest.
Hermani teooria leidis eksperimentaalset kinnitust.
Helmholtz – määras konnas impulsi levimiskiiruse; Babsky - määras inimeses impulsi leviku kiiruse. Erlander ja Gasser klassifitseerisid erinevad närvikiud kolme rühma: A, B ja C:
Närvikiudude tüübid
A - müeliniseerunud, suurim läbimõõt, kiirus 120-70 m sekundis, AP kestus - minimaalne, jagatud alarühmadesse: alfa, beeta, gamma, delta. Näiteks võib tuua motoorsete neuronite aksonid.
B - müeliniseerunud kiud, väiksem läbimõõt, kiirus 3-18 m sekundis, AP on pikem. Näiteks on sümpaatilise närvisüsteemi preganglionilised kiud.
C - mittemüeliseeritud närvikiud, kiirus alla 2 m sekundis, AP kestus on pikim. Näiteks on parasümpaatilise närvisüsteemi postganglionilised kiud.
Ergutuse juhtivuse seadused piki närve.
ma seadusnärvikiu anatoomiline ja füsioloogiline terviklikkus. Ergastuse levimiseks piki närvikiudu on vajalik mitte ainult selle morfoloogiline terviklikkus, vaid ka füsioloogiline järjepidevus. Ettevalmistused juhtivuse anesteesiaks rikuvad füsioloogilist järjepidevust, inaktiveerides närvikiudude naatriumi läbilaskvust.
II seadusergastuse isoleeritud juhtivus piki närvikiudu. Seganärvi korral ei kandu erutus ühest närvikiust naaberkiududele, kuna rakkudevahelise vedeliku takistus on väiksem kui naaberkiudude membraanide takistus. See tagab info edastamise täpsuse närvikiududes innerveeritud struktuuridele.
III seadus ergastuse kahepoolne juhtivus. AP levimine piki närvikiudude membraani on võimalik mõlemas suunas, kuna membraani struktuur on läbivalt sama. Samal ajal ei saa erutus naasta piirkonda, kust see tekkis, kuna see on tulekindlas seisundis.
Parabioos. MITTE. Vvedensky, uurides impulsi läbimist närvisegmendi kaudu, mida mõjutavad keemilised või narkootilised ained (muundurid), täheldas labiilsuse järsku vähenemist. Parabioosi iseloomustab järkjärguline areng, milles saab eristada nelja faasi:
I Prodromaal (mitte alati avaldub, kuna see on väga lühiajaline) iseloomustab: suurenenud erutuvus, suurenenud labiilsus.
II Tasakaalustamine – tugevate ja nõrkade stiimulite mõju on tasakaalus.
III Paradoksaalne - tugevate või sagedaste ärrituste korral on mõju nõrgem kui nõrkade või haruldaste ärrituste korral.
IV Inhibeeriv – ei tugevad ega nõrgad ärritused ei põhjusta lihaskontraktsioone. Impulsid ei läbi kahjustatud piirkonda.
Kui kahjustatud alale mõjub teine elektroodide paar, siis tekib erutus, s.t. kude on veel elus.
Alteraatori eemaldamisel naaseb kude oma algsesse olekusse IV, III, II, I faaside vastupidises järjekorras.
Parabioos on püsiv mittelevitav erutus.
Esineb amplituudilt väiksemaid potentsiaale ja seejärel katkevaid potentsiaale, mis ei ole võimelised levima: Na läbilaskvuse protsessid vähenevad ja Na inaktiveerimise protsessid suurenevad.
neuromuskulaarne ülekanne.
Inimese suhtlemist väliskeskkonnaga ei saa ette kujutada ilma tema lihaskonnata. Skeletilihaste liigutused on vajalikud nii lihtsaimate kehaliigutuste tegemiseks ruumis, kirurgi, hambaarsti keerukateks manipulatsioonideks, peenemate tunnete ja mõtete väljendamiseks kõne, näoilmete ja žestide kaudu. Südame töö tagab kõigi elundite verevarustuse, silelihaste töö loob tingimused füsioloogiliste protsesside normaalseks läbiviimiseks, mis tagavad homöostaasi peaaegu kõigis süsteemides: seedetraktis, südame-veresoonkonnas, eritus-, reproduktiiv-, hingamissüsteemis. Skeletilihaste juhtiv roll on ka soojuse tootmisel ja kehatemperatuuri hoidmisel. Lihased on "masinad", mis muudavad keemilise energia mehaaniliseks (tööks) ja soojuseks. Lihasmass on suurem kui teistel organitel, 40-50% kehakaalust.
Looduslikes tingimustes (meie kehas) toimub lihaskiu (või mitme lihase moodustava lihaskiu) ergastumine närvikiudude ergastuse ülekandumise tulemusena lihasmembraanile nende kokkupuutepunktides. närv ja lihased: neuromuskulaarsed sünapsid.
Neuromuskulaarse ülekande mehhanism
Sünapsid on sidestruktuurid, mis moodustuvad närvikiu otsast ja külgnevast lihaskiu membraanist (presünaptilised närvi- ja postsünaptilised lihasmembraanid) (joonis 2). 
Joonis 2. mioneuraalne sünaps.
Kui närviimpulss jõuab aksoni lõpuni, avanevad depolariseeritud presünaptilisel membraanil pingepõhised Ca2+ kanalid. Ca2+ sisenemine aksoni pikendusse (presünaptilisse membraani) soodustab keemiliste neurotransmitterite vabanemist, mis on vesiikulite (vesiikulite) kujul aksoni otsast. Vahendajad (neuromuskulaarses sünapsis on selleks alati atsetüülkoliin) sünteesitakse närviraku somas ja transporditakse aksonaalse transpordi teel aksoni lõppu, kus nad täidavad oma rolli. Vahendaja difundeerub läbi sünaptilise pilu ja seondub postsünaptilise membraani spetsiifiliste retseptoritega. Kuna neuromuskulaarse sünapsi vahendajaks on atsetüülkoliin, nimetatakse postsünaptilise membraani retseptoreid kolinergilisteks retseptoriteks. Selle protsessi tulemusena avanevad postsünaptilisel membraanil kemosensitiivsed Na + kanalid, toimub depolarisatsioon, mille suurus on erinev ja sõltub vabaneva mediaatori kogusest. Kõige sagedamini toimub lokaalne protsess, mida nimetatakse otsaplaadi potentsiaaliks (EPP). Närvikiudude stimulatsiooni sageduse suurenemisega suureneb presünaptilise membraani depolarisatsioon ja sellest tulenevalt suureneb vabanenud mediaatori hulk ja aktiveeritud kemosensitiivsete Na + kanalite arv postsünaptilisel membraanil. Seega tekivad PKP, mis depolarisatsiooni amplituudi osas summeeritakse lävitasemeni, mille järel sünapsi ümbritseva lihaskiu membraanil tekib AP, millel on võime levida mööda lihase membraani. kiudaineid. Postsünaptilise membraani tundlikkust reguleerib ensüümi atsetüülkoliinesteraasi (ACCh-E) aktiivsus, mis hüdrolüüsib ACh vahendaja selle koostisosadeks (atsetüül ja koliini) ning tagastab selle taassünteesiks presünaptilisse naastu. Ilma vahendaja eemaldamiseta areneb postsünaptilisel membraanil pikaajaline depolarisatsioon, mis põhjustab sünapsi ergastuse juhtivuse katkemise - sünaptilise depressiooni. Seega tagab sünaptiline ühendus ergastuse ühesuunalise ülekande närvist lihasesse, kuid kõik need protsessid võtavad aega (sünaptiline viivitus), mis põhjustab sünapsi madala labiilsuse võrreldes närvikiuga.
Seega neuromuskulaarne sünaps on "hea koht mida saab mõjutada farmakoloogiliste preparaatidega, muutes retseptori tundlikkust, ensüümi aktiivsust. Selliseid nähtusi esineb sageli arstide praktikas: näiteks botulismitoksiiniga mürgituse korral on ACH-i vahendaja vabanemine blokeeritud (kosmeetilises meditsiinis kortsude silumine), kolinergiliste retseptorite blokaad (kurare-sarnaste ravimitega, bungarotoksiin) häirib Na + kanalite avanemist postsünaptilisel membraanil. Fosfororgaanilised ühendid (paljud insektitsiidid) vähendavad ACH-E efektiivsust ja põhjustavad postsünaptilise membraani pikaajalist depolarisatsiooni. Kliinikus kasutatakse spetsiifilisi neuromuskulaarse juhtivuse blokaatoreid: kolinergiliste retseptorite blokeerimine curare-sarnaste ravimitega, suktsinüülkoliini ja teiste konkureerivate inhibiitoritega, mis tõrjuvad ACh kolinergiliselt retseptorilt välja. Myasthenia gravis'e korral tekib postsünaptilise membraani kolinergiliste retseptorite puudulikkuse tõttu (nende autolüütilise hävimise tõttu) progresseeruv lihasnõrkus kuni lihaste kontraktsioonide täieliku peatumiseni (hingamise seiskus). Sel juhul kasutatakse ACH-E blokaatoreid, mis viib vahendaja sidumise kestuse pikenemiseni väiksema arvu kolinergiliste retseptoritega ja suurendab veidi postsünaptilise membraani depolarisatsiooni amplituudi.
Lihaste füsioloogia.
Lihaskudesid on kolme tüüpi: vööt-, südame- ja silelihaskude.
Skeleti lihaskude moodustab suure hulga somaatilisi lihaseid. See sisaldab kontraktiilsete valkude täpselt määratletud järjestatud struktuuri põikitriibutuse kujul. Üksikute lihaskiudude vahel pole seoseid. Kokkutõmbumist juhitakse teadlikult.
Südamelihasesse sisaldab ka põiktriibutust, kuid on funktsionaalne süntsütium. Südamestimulaatori rakkude olemasolu tõttu on sellel võime tekitada spontaanseid närviimpulsse, mis tagavad südame kokkutõmbed.
AT sile lihastes ei esine põiktriibutust, mis annaks sellele koele teatud füüsikalised ja füsioloogilised omadused. Niisiis, erinevalt skeletilihastest, mida iseloomustab kõrge elastsus, on silelihastes plastilisuse omadus rohkem väljendunud, mis on tingitud aktiini ja müosiini müofilamentide selge järjestuse puudumisest. Erinevalt skeleti- ja südamelihase tavalisest sarkomeerilisest struktuurist kinnituvad õhukesed silelihase filamendid tsütoplasmas olevate struktuuride külge, nn. tihedad kehad(sarcolemma kinnitusnaastud), mis koosnevad valgust desmina. Siledad lihased on vistseraalne (mitmeühtne) ja polüelementaarne (ühtne).
Vistseraalne sisaldavad sildu - lünkkontakte madala takistusega elektrivoolule - süntsütiumi. Vistseraalsed lihased asuvad õõnsate organite (sooled, emakas, kusejuhad, põis) seintes.
Polüelement silelihased koosnevad eraldiseisvatest lihasüksustest ilma ühendavate sildadeta, seetõttu iseloomustavad neid täpsed, hästi doseeritud kontraktsioonid, nagu skeleti omad. Erinevalt skeletilihastest (iirise, ripskeha, seemnejuhade, arterite lihased) ei saa nende lihaste kokkutõmbeid siiski kontrollida. Oma struktuuri tõttu (vistseraalne) neil on suur plastilisus, kuid teatud piiratud venitusastmel on nad võimelised depolariseeruma ja kokku tõmbuma (iseregulatsioon). Näiteks põie seinte sees muutub rõhk suhteliselt väikese venitusega vähe, kui venitus suureneb järsult - detruusorlihased tõmbuvad kokku - uriin evakueeritakse ka juhtudel, kui innervatsioon on häiritud. Polüelement silelihastel on võimsam (tihedam) innervatsioon ja rakkudevaheliste kontaktide (nexuse) nõrk areng. Nende lihaste toonus ja selle kõikumised on oma olemuselt neurogeensed. Neil on parasümpaatilised ja sümpaatilised, samuti metasümpaatilised kiud. Silelihaste närvilõpmete struktuur erineb skeletilihaste neuromuskulaarse sünapsi struktuurist. Silelihasel puuduvad otsaplaadid ja üksikud närvilõpmed. Adrenergiliste ja kolinergiliste närvikiudude hargnemise kogu pikkuses on paksenemised, mida nimetatakse veenilaienditeks. Need sisaldavad graanuleid koos vahendajaga, mis vabaneb igast veenilaiendist. Rakke, millel puudub otsene kontakt veenilaiendite veenidega, aktiveerivad PD-d, mis levivad sidemete kaudu naaberrakkudesse. Närvikiu käigus saab lihasrakke ergastada või pärssida (adrenergiliste kiudude stimuleerimine väheneb ja kolinergilised kiud suurendavad lihaste aktiivsust, teistes nt veresoontes suurendab norepinefriin, atsetüülkoliin vähendab lihastoonust. Iooniline olemus silelihaste ioonide määravad membraanikanalite omadused Ca2+ ioonid mängivad peamist rolli AP tekke mehhanismis, kuid nende kanalite kaudu võivad rakku liikuda ka teised kahevalentsed ioonid Ba2+, Mg2+. Ca2+ sisenemine rakku on vajalik selleks, et säilitada lihastoonust ja arendada kontraktsioone, mistõttu silelihaste Ca2+ kanalite blokeerimine piirab selle iooni sisenemist siseorganite ja veresoonte müotsüütide tsütoplasmasse, mida praktilises meditsiinis laialdaselt kasutatakse lihaste motoorsete funktsioonide korrigeerimiseks. seedetrakti ja veresoonte toonust.
Lihaste kontraktsioonide reguleerimine sõltub innervatsiooni mahust. Seljaaju (motoorse) motoneuroni akson hargneb mitmeks terminaliks (haruks), millest igaüks läheneb ühele lihaskiule. Seetõttu väheneb terves organismis 1 närvikiu ergastamisel mingi lihasrühm. Motoorse neuroni ja selle innerveeritavate lihaskiudude kombinatsiooni nimetatakse motoorseks üksuseks. Motoorses üksuses sisalduvate lihaskiudude arv on erinev ja sõltub funktsioonist, mida iga konkreetne keha lihas täidab. Silmade, käte lihastes, mis tagavad ülitäpsed, koordineeritud liigutused, sisaldab 1 motoorne üksus 3-5 lihaskiudu. Selja, reie lihaste motoorsed üksused - koosnevad mitmesajast lihaskiust, mida reguleerib üks motoorne neuron.
Pöördugem tagasi lihaskiudude membraani juurde, millel AP levib, mis tuleneb ergastuse "edukast" juhtimisest läbi sünapsi. Lihaskiudude membraani jätkuks on sarkotubulaarne süsteem, mis moodustab põiki invaginatsioonid (invaginatsioonid) (T-süsteem risttuubulitest). T-tuubulite süsteem täidab mitmeid olulisi funktsioone: see on rakusisene Ca2+ ioonide depoo; suhtleb rakuvälise vedelikuga ja reguleerib seeläbi Ca2+ sisaldust selles; sisaldab pingetundlikke Na+ kanaleid, mis võimaldavad AP-l levida nii piki lihaskiudu kui ka sügavale sellesse. T-tuubulite süsteem tagab lihasraku kiire ja koordineeritud ergutamise, kuna depolarisatsiooni levik mööda T-süsteemi on seotud Ca2+ vabanemisega sarkoplasmaatilise retikulumi tsisternidest ja annab lihaskontraktsiooni algatamise. T-tuubulite kaudu võivad ainevahetusproduktid (näiteks piimhape) vabaneda lihasrakust interstitsiumi (rakkudevahelisse ruumi) ja sealt edasi verre. Skeletilihasraku suurt mahtu ei saaks kiiresti aktiveerida, kui Ca2+ tarniti rakuvälisest keskkonnast. Ca2+ akumuleerumist sarkoplasmaatilises retikulumis soodustab valk (kalsekvestriin), mis seob lõdvalt Ca2+ retikulumis. Ca2+ vabanemine skeletilihaste sarkoplasmaatilisest retikulumist toimub T-tuubulite ja terminaalsete tsisternide (triaadi) interaktsiooni tõttu.
Sarkoplasmasse sattudes algatavad Ca2+ ioonid kontraktsiooni, seondudes puhkeolekus aktiini blokaatori troponiini valguga (joonis 3).

Pilt. 3. Lihaste kokkutõmbumise mehhanism.
Õhuke aktiini filament koosneb 2 fibrillaarse aktiini ahelast, millele on keerdunud eraldi aktiini monomeeri gloobulid (nagu helmed). Aktiin sisaldab müosiiniga seondumiseks aktiivseid keskusi (saite), mida puhkeolekus troponiin blokeerib. Tropoonium pärsib müosiini ATP-aasi aktiivsust, mistõttu ATP lagunemine on võimatu ja lihaskiud on lõdvestunud. Suur kontraktiilne valk on müosiin, mis koosneb 6 paarikaupa virnastatud polüpeptiidahelast. 2 neist on müoglobiini rasked ahelad, millel on ensüümide omadus. Trononiiniga seotud Ca2+ vabastab aktiini aktiivsed saidid kokkupuuteks müosiiniga. Aktiini juuresolekul lõhustab müosiini ensüüm (kerakujuline pea) ATP-d ja interakteerub aktiini õhukeste filamentidega, luues kokkutõmbumise liikumapaneva jõu - moodustades põikisildu (“löögid”) ja lihased lühenevad (kokkutõmbuvad). Seega annab ATP energiat kokkutõmbumiseks, hüdrolüüsides müosiini kerakujulistel peadel. Energia (E), mis vabaneb ATP hüdrolüüsi käigus, muudetakse kontraktsioonijõuks müosiini konformatsiooniliste (ruumiliste) muutuste tõttu (töökäik – põiki aerusildade moodustumine) – see on aktivatsioonisoojus, mis vabaneb aktiini ja müosiini siduda. Müosiiniga seotud ADP vähendab ristsilla afiinsust aktiini aktiivse saidi suhtes, mis käivitab järgmise faasi – lihaste lõdvestumise. ATP hüdrolüüsi tõttu eraldub E (lühenemissoojus), mis läheb:
1) Ca-ATPaasi töö (pumba aktiveerimine toimub ATP hüdrolüüsi käigus tekkiva anorgaanilise fosfaadi tõttu),
2) tänu E-le pumbatakse Ca2+ kontsentratsioonigradiendi vastu tagasi sarkoplasmaatilisesse retikulumi (aktiivne transport).
3) Lihasrakus olev ATP tagab Na+-K-ATP-aasi töö, mis eemaldab rakust Na+ ja taastab lihasraku puhkepotentsiaali (ja sellest tulenevalt ka erutatavuse).
ATP tagab nii kontraktsiooni kui ka lõõgastumise protsessid. Kui Ca2+ ei transpordita tagasi SR-i, siis lõdvestumist ei toimu, tekib lihasrigiidsus (koos rigor mortisega) või elusorganismis - post-teetanilise kontraktuuriga - algatab Ca2+ kogunemine sarkoplasmasse pikaajalise lihase. kontraktsioon väljaspool AP tarnimist sünapsi kaudu lihaskiudude membraanile.
Silelihas sisaldab ka tropomüosiini, kuid ei sisalda troponiini, aktiini ja müosiini suhe on 14-16:1, võrrelge skeletis aktiini ja müosiini suhet 2:1. Silelihasel on vaheühendused - need on membraane ühendavad sillad naaberrakkudest. Silelihaste kontraktiilse aktiivsuse reguleerimine toimub tänu Ca2+ seondumisele kalmoduliiniga, mis aktiveerib müosiini kerge ahela kinaasi, mis viib ATP hüdrolüüsini ja käivitab ristsilla moodustumise tsükli.
Skeletilihase AP kestab umbes 2–4 ms ja läbib lihaskiudmembraani kiirusega umbes 5 m/s. 1 AP põhjustab ühe lihase kontraktsiooni, mis algab 2 ms pärast membraani depolarisatsiooni (latentse perioodi) algust ja lõpeb peaaegu samaaegselt repolarisatsiooniga. Ühekordse kontraktsiooni kestus on erinev ja sõltub lihaskoe tüübist. Sagedaste stiimulite korral tekib lihaste totaalne kontraktsioon kõigis erineva membraani takistusega elektrivoolule lihaskiududes. Väikesed erinevused ergastuse lävedes tagavad aga kogu lihase lihaskontraktsiooni sünkroonsuse. Umbes 1-3 ms pikkune absoluutne refraktaarne periood põhjustab erinevat tüüpi teetanuse (lihaste kogukontraktsioonide) esinemist. On dentate ja sile teetanus. Lihasstimulatsiooni sagedus sileda teetanuse tekkeks peab olema suurem kui hambulise tekkeks. Stiimul peaks langema lihaste lühenemise faasi, kuid kui lihased hakkavad lõdvestuma ja me stimuleerime seda, siis saame teetanuse hambulise. Minimaalne ajavahemik järjestikuste tõhusate stiimulite vahel teetanuse ajal ei saa olla lühem kui refraktaarne periood, mis vastab ligikaudu AP kestusele. Kuna lihased koosnevad erineva erutuvuse tasemega lihaskiududest, on stiimuli suuruse ja reaktsiooni vahel kindel seos. Kontraktsioonijõu suurenemine on võimalik teatud piirini, pärast mida jääb kokkutõmbumise amplituud stiimuli amplituudi suurenemisega muutumatuks (tuleb märkida, et lihases summeeritakse mitte AP, vaid kontraktsioonid) . Sel juhul võtavad kokkutõmbumisest osa kõik lihase moodustavad kiud.
Inimese kehas on kiired, faasilised lihaskiud (valged), mille kestus on kuni 7,5 ms, ja aeglased, toniseerivad (punased), mis annavad tugevaid ja jõulisi liigutusi, mis kestavad kuni 100 ms. Punasel (toonikul) on palju I tüüpi müosiinkiude, mida iseloomustab müosiini ATPaasi madal aktiivsus. ATP lõhenemise kiirus on tegur, mis määrab insuldi liigutuste sageduse ja seega ka aktiini filamentide libisemise kiiruse mööda müosiini. SPR-st transporditakse Ca2+ aeglaselt, kõrge oksüdatsioonivõime, palju kapillaare, palju müoglobiini müosiini struktuuris (rasked ahelad), palju mitokondreid. Nad reageerivad stiimulile aeglaselt, neil on pikk varjatud kokkutõmbumisperiood, mistõttu nad on võimelised pikkadeks, aeglasteks, toonilisteks kontraktsioonideks ja on vastupidavamad väsimusele. Peamine ülesanne on keha asendi säilitamine. Valged lihased sisaldavad II tüüpi müosiini kiude. Glükolüütiline oksüdatsioonitüüp, vähe müoglobiini, mitokondrid, need on suure läbimõõduga kiud, millel on kõrge müosiini ATPaasi aktiivsus, mis on võimelised arendama märkimisväärset tugevust, kuid väsivad kiiresti.
lihasjõud määratakse maksimaalse koormuse järgi, mida lihas suudab veidi tõsta. Erinevate lihaste tugevus ei ole sama. Erinevate lihaste tugevuse võrdlemiseks jagatakse maksimaalne koormus, mida lihas suudab tõsta, selle füsioloogilise ristlõike ruutsentimeetrite arvuga. Tugevusnäitajad on kõrgemad lihaste puhul, mille kiudude paigutus on kaldus, samas kui füsioloogiline ristlõige on suurem kui geomeetriline ristlõige. Ristlõike summa ei lange alati kokku lihase füsioloogilise lõiguga (ainult siis, kui kiud on paralleelsed.
kokkutõmbumisjõud isoleeritud skeletilihase suurus, kui muud tegurid on võrdsed, sõltub lihase esialgsest pikkusest. Lihase mõõdukas venitamine põhjustab selle poolt arendatud jõu suurenemist võrreldes venitamata lihase poolt arendatava jõuga. Lihase elastsete komponentide olemasolu ja aktiivse kontraktsiooni tõttu on passiivne pinge liitmine (üleminek keskmiste koormuste reeglile on selle seaduse füsioloogiline mehhanism). Oskus pühenduda tööd määratakse tõstetud koorma väärtuse ja tõstekõrguse korrutisega. Lihastöö maht suureneb järk-järgult tõstetava koormuse massi suurenemisega, kuid teatud piirini, mille järel koormuse massi suurenemine toob kaasa töömahu vähenemise, kuna koormus langeb järsult. Seetõttu teeb maksimaalse töö ära lihas, kui keskmised koormused. Kokkutõmbumisjõud ja töö ei jää staatilise ja dünaamilise töö puhul konstantseks. Pikaajalise tegevuse tulemusena väheneb skeletilihaste töövõime. Seda nähtust nimetatakse väsimus. Samal ajal väheneb kontraktsioonide tugevus, suureneb varjatud kontraktsiooniperiood ja lõõgastusperiood. Staatiline töörežiim on tüütum kui dünaamiline režiim (miks seda seletada). Oksüdatsiooniprotsesside produktid kogunevad - piimpüroviinamarihape, mis vähendab PD tekke võimalust. Häiritud on ATP ja kreatiinfosfaadi resünteesi protsessid, mis on vajalikud lihaste kontraktsioonide energiaga varustamiseks. Looduslikes tingimustes määrab lihaste väsimuse staatilise töö ajal peamiselt ebapiisav piirkondlik verevool. Tekib "hapnikunälg" ja väsimus suureneb järk-järgult.
1903. aastal Sechenov - väsinud lihase jõudluse taastamine kiireneb oluliselt, kui väsinud lihase puhkeperioodil teeb tööd mõni teine lihas - näiteks puhkust nimetatakse aktiivseks. Kõrge vaimne aktiivsus aga kiirendab väsimuse teket lihassüsteemis (närvikeskuste väsimus).