Valgud on looduslikud polümeerid, mis koosnevad jääkainetest. Bioloogilised polümeerid – valgud
Keemia esitlus
teemal:
"Oravad -
loomulik
polümeerid"

VALGUD on keerulise koostise ja molekulaarstruktuuriga lämmastikku sisaldavad makromolekulaarsed orgaanilised ained.
Valku võib pidada aminohapete keeruliseks polümeeriks.
Valgud on osa kõigist elusorganismidest, kuid eriti olulist rolli mängivad nad loomorganismides, mis koosnevad mitmesugustest valkude vormidest (lihased, sisekuded, siseorganid, kõhre, veri).

iseloomulik tunnus valkude mitmekesisus on seotud
nende molekulis sisalduv arv, omadused ja ühendusviisid
aminohapped.
Valkude koostis sisaldab 20 erinevat aminohapet, seega tohutu valik valke koos erinevate aminohapete kombinatsioonidega. Kuidas teha tähestiku 33 tähest lõpmatu arv sõnu, seega 20 aminohappest – lõpmatu hulk valke. Inimese kehas on kuni 100 000 valku.

Taimed sünteesivad valke sellest süsinikdioksiid CO2 ja vesi H2O fotosünteesi teel, assimileerides pinnases lahustuvatest sooladest ülejäänud valkude elemendid (lämmastik N, fosfor P, väävel S, raud Fe, magneesium Mg).
Loomorganismid saavad valmis aminohappeid peamiselt koos toiduga ja nende pealt
Aluse ehitavad üles teie keha valgud. Mitmed aminohapped (mitteasendatavad aminohapped)
saab sünteesida otse loomsete organismide poolt.

Valkude struktuur
Valgud on ebakorrapärased polümeerid, mis on ehitatud aminohappejääkidest.
Valkude aminohappejäägid on ühendatud amiidsidemega amino- ja karboksüülrühmade vahel. Kahe aminohappejäägi vahelist seost nimetatakse tavaliselt peptiidsidemeks ja polümeere, mis on ehitatud peptiidsidemetega ühendatud aminohappejääkidest, nimetatakse polüpeptiidideks.
Seega on valk polüpeptiid, mis sisaldab sadu või
tuhandeid aminohappeid.
Valk kui bioloogiliselt oluline struktuur võib olla kas üks polüpeptiid või mitu polüpeptiidi, mille tulemuseks on
mittekovalentsed interaktsioonid üks kompleks.

Natuke ajalugu..
Ajaloo viide.
Esimene hüpotees valgu molekuli struktuuri kohta esitati XIX sajandi 70ndatel. See oli valgu struktuuri ureide teooria. 1903. aastal pakkus saksa teadlane E. G. Fischer välja peptiiditeooria, millest sai valgu struktuuri mõistatuse võti. Fisher väitis, et valgud on aminohappejääkide polümeerid, mis on ühendatud NH-CO peptiidsidemega.
Idee, et valgud on polümeersed moodustised, väljendas juba 1888. aastal vene teadlane A. Ya Danilevsky. Polüpeptiiditeooria järgi on valkudel kindel struktuur. Rakk sisaldab vabu aminohappeid, mis moodustavad aminohappekogumi, mille tõttu sünteesitakse uusi valke. Seda fondi täiendatakse aminohapetega, mis sisenevad pidevalt rakku toiduvalkude lagunemise tulemusena seedeensüümide või nende enda säilitusvalkude poolt.
E.G.Fischer
A. Ja. Danilevski

Klassifikatsioon
Valgud jagunevad valkudeks ( lihtsad valgud) ja proteiinid (kompleksvalgud)

Valkude funktsioonid
Valkude funktsioonid.
Kaitske keha mikroobide ja viiruste eest, osaledes antikehade tootmises;
Reguleerige energiabilanssi, eriti kui rasked koormused või rasvade ja süsivesikute puudusega dieedis.
Tagage keha kasvu, paljunemise ja täieliku arengu, eriti närvisüsteem, reguleerides ärrituvust ja reaktsioone välistele stiimulitele;
Need on osa hormoonidest, lihastest ja muudest kudedest;
Seoses vitamiinide ja mikroelementidega on need bioloogilised katalüsaatorid – ensüümid;
Need moodustavad aine liikumise kõrgeima vormi – mõtlemise – võime;

Elementaarne koostis
valgud
Valkude elementaarne koostis
23% hapnikku, 6-7% vesinikku, 0,3-2,5% väävlit.
Üksikute valkude koostises leidus ka fosforit, joodi, rauda, vaske ja mõningaid teisi makro- ja mikroelemente, erinevates, sageli väga väikestes kogustes.
välja arvatud lämmastik, mille kontsentratsiooni iseloomustab kõrgeim
püsivus.

Valkude struktuur
Iga liigi valgu eripära ei ole seotud mitte ainult selle molekulis sisalduvate polüpeptiidahelate pikkuse, koostise ja struktuuriga, vaid ka nende ahelate orientatsiooniga.
Mis tahes valgu struktuuris on mitu organiseerituse astet:
Valkude esmane struktuur
1 . Valgu esmane struktuur- spetsiifiline aminohapete järjestus polüpeptiidahelas.
Isegi kui need on ühepikkused ja aminohapete koostis peptiidid võivad olla erinevad ained, kuna aminohapete järjestus ahelas on erinev.

Valkude sekundaarne struktuur
Valgu sekundaarne struktuur on viis, kuidas polüpeptiidahelasse keeratakse
ruum (mis on tingitud vesiniksidemest amiidrühma -NH- vesiniku ja
karbonüülrühm - CO-, mis on eraldatud nelja aminohappega
killud).
Samas valgus võivad esineda kõik kolm polüpeptiidahela voltimise viisi:
Sekundaarne struktuur on spiraal, mille pöörete vaheline kaugus on sama.
Valkude tertsiaarne struktuur
Valgu tertsiaarne struktuur on polüpeptiidahela keerdunud spiraali ruumis (heeliksiks keerdunud heeliksi) tõeline kolmemõõtmeline konfiguratsioon.
Valgu tertsiaarne struktuur määrab valgu molekuli spetsiifilise bioloogilise aktiivsuse. Valgu tertsiaarne struktuur säilib polüpeptiidahela erinevate funktsionaalrühmade interaktsiooni kaudu:
disulfiidsild (-S-S-) väävliaatomite vahel,
estersild - karboksüülrühma (-CO-) ja
hüdroksüül (-OH),
soolasild - karboksüül- (-CO-) ja aminorühmade (NH2) vahel.

Kvaternaarne valgu struktuur
Valgu kvaternaarstruktuur – mitmete interaktsioonide tüüp
polüpeptiidahelad.
Näiteks hemoglobiin on neljast makromolekulist koosnev kompleks
Füüsikalised omadused
Valkudel on suur molekulmass (104-107),
paljud valgud lahustuvad vees, kuid moodustavad tavaliselt kolloidseid lahuseid, millest sadestuvad anorgaaniliste soolade kontsentratsiooni suurenemisel, raskmetallide soolade, orgaaniliste lahustite lisamisel või kuumutamisel.
Valgud on võimelised paisuma, neid iseloomustab optiline aktiivsus ja liikuvus elektriväljas, mõned on vees lahustuvad. Valkudel on isoelektriline punkt.

Keemilised omadused
Valkude kõige olulisem omadus on nende võime eksponeerida mõlemat
happelised ja aluselised omadused, st toimivad amfoteersena
elektrolüüdid.

Kinnistu a mfoterism on valkude ja nende puhverdusomaduste aluseks
osalemine vere pH reguleerimises.

Keemilised omadused
2. Kvalitatiivsed reaktsioonid valkudele:
biureedi reaktsioon: violetne värvus, kui seda töödeldakse leeliselises keskkonnas vasesooladega (annab kõik valgud),
ksantoproteiini reaktsioon: kollane värv tegevusel
kontsentreeritud lämmastikhape, mis muutub toimel oranžiks
must sade(sisaldab väävlit) pliiatsetaati lisamisega
(II) naatriumhüdroksiid ja kuumutamine.
- Denatureerimine - valgu sekundaarse ja tertsiaarse struktuuri hävitamine.
pöördumatu denaturatsioon
orav kana muna mõju all kõrge temperatuur

3. Valkude hüdrolüüs - kuumutamisel aluselises või happelises lahuses koos
aminohapete moodustumine.
Hüdrolüüsireaktsioon aminohapete moodustumisega üldine vaade võib kirjutada nii:

Põlemine
Valgud põlevad koos lämmastiku, süsihappegaasi ja vee, aga ka mõne muu aine moodustumisega. Põlemisega kaasneb põlenud sulgedele iseloomulik lõhn.

Valkude süntees
Otsides võimalusi valgu kunstlikuks saamiseks, uurivad teadlased intensiivselt selle sünteesi mehhanismi organismides. Siin toimub ju see "pehmetes" tingimustes, üllatavalt selgelt ja koos suur kiirus. (Valgu molekul moodustub rakus vaid 2-3 sekundiga.)
Leiti, et valkude süntees kehas toimub teiste makromolekulaarsete osavõtul.
nukleiinhapped.
Praegu on inimene juba sügavalt mõistnud valkude biosünteesi mehhanismi ja hakanud kunstlikult hankima kõige olulisemat.
valke samade põhimõtete alusel, mis on nii suurepäraselt välja töötatud
orgaanilise maailma areng.

Järeldus
Selles töös on keemiline ja füüsikalised omadused käsitleti valke, valkude klassifikatsiooni, valkude koostist ja struktuuri, valkude erinevaid funktsioone, aga ka nende tähtsust.
On tõestatud, et valgud on hädavajalikud komponent kõigist elusrakkudest mängivad eluslooduses äärmiselt olulist rolli, on toitumise peamine, väärtuslikum ja asendamatu komponent. See on tingitud nende tohutust rollist arenguprotsessides ja inimelus. Valgud on aluseks konstruktsioonielemendid ja kudesid, toetavad ainevahetust ja energiat, osalevad kasvu- ja paljunemisprotsessides, tagavad liikumismehhanismid, immuunreaktsioonide kujunemise, on vajalikud kõigi organismi organite ja süsteemide tööks.
"Elu on valgu olemasolu vorm"

VENEMAA FÖDERATSIOONI HARIDUSMINISTEERIUM
ALTA RIIKLIKÜLIKOOL
Keemiateaduskond
Kursuse töö
Teema:Polümeeride struktuur, biopolümeerid
Valkude struktuur
Töö lõpetatud:
4. kursuse üliõpilane
Kontrollitud:
Ph.D., dotsent
"___" _____________ 2002
Hinne________________
_______________________
(juhi allkiri)
Barnaul 2002
1. Mis on polümeer?. neli
1.1. Polümeeride struktuuri tunnused. neli
2. Looduslikud polümeerid.. 6
2.1. kiudaineid. 6
2.2. Kumm. 7
2.3. Bioloogilised polümeerid... 7
3. Sünteetilised polümeerid.. 8
3.1. kiudaineid. kaheksa
3.2. kummid. 9
3.3. Kristallilised polümeerid.. 10
3.4. Klaasid ja vaigud.. 10
4. Keskmised molekulmassid.. 11
5. Konfiguratsioon, stereokeemia ja ahela konformatsioon. 12
6. Polümeeride klassifikatsioon. viisteist
7. Termilised üleminekud polümeerides. kaheksateist
8. Valgud. kakskümmend
9. Keemilised sidemed valgu molekulis. 21
10. Valgu molekuli struktuurse organiseerituse tasemed. 23
10.1. esmane struktuur. 23
10.2. sekundaarne struktuur. 25
10.2.1. a-spiraal. 25
10.2.3. Kollageeni spiraal. 27
10.2.4. Supersekundaarsed struktuurid ja struktuurivaldkonnad.. 27
10.3. Tertsiaarne struktuur. 27
10.4. Kvaternaarne struktuur. 29
Kirjandus. 31
1. Mis on polümeer?
1.1. Polümeeride struktuuri tunnused
Sõna "polümeer" tähendab sõna otseses mõttes - palju segmente (kreeka keelest polus- palju ja teros-osad, segmendid).
See mõiste hõlmab kõiki aineid, mille molekulid on üles ehitatud paljudest elementidest või lülidest. Need elemendid hõlmavad nii üksikuid aatomeid kui ka (sagedamini) väikeseid keemiliste sidemetega ühendatud aatomite rühmi. Elementaaraatomitest koosnevate elementidega polümeeri näide on niinimetatud "plastiline väävel". See saadakse sulaväävli (sobival temperatuuril) valamisel külm vesi. Polümeerse väävli struktuuri võib kujutada aatomite ahelana, mis on omavahel keemiliste sidemetega seotud
Sellises olekus on väävli füüsikalised omadused erinevad tavalise kristallilise või kivimi väävli omadest – need on tüüpilisemad kummitaolistele polümeeridele. Pehme, väga elastne ja poolläbipaistev, erinevalt kristalsetest ainetest ei ole sellel kindlat sulamistemperatuuri. Temperatuuri tõustes väävel esmalt pehmeneb ja seejärel voolab väga viskoosse vedelikuna. Polümeerne väävel ei ole aga stabiilne isegi temperatuuril toatemperatuuril mõne päeva pärast taastub see tavalisele pulbrilisele või kristallilisele kujule.
Enamiku polümeeride puhul on struktuuri korduvaks elemendiks väike teatud viisil ühendatud aatomite rühm. Keemilise struktuuri poolest üks lihtsamaid polümeere - polüetüleenil on korduva elemendina CH2 rühm.
Algmolekuli, millest polümeer moodustub, nimetatakse monomeerühikuks (kreeka keelest monod- vallaline). Nagu see näide näitab, ei ole monomeerüksus alati korduv ahelelement.
Kuid ketilülid ei ole alati identsed. Paljud polümeerid moodustuvad kahe koosmõjul mitmesugused monomeerühikud või keemilised ühendid. Selle tulemuseks on struktuur nagu
http://pandia.ru/text/78/042/images/image002_56.gif" width="333" height="19 src=">
See struktuur on tüüpiline paljudele sünteetilistele kummidele.
Üks lülidest, näiteks B, võib ühenduda A-ga mitte ainult otstes, vaid ka kolmandas punktis. See võimaldab ahelatel hargneda:

Selline polümeer võib "kasvada" igast hargnemiskohast, moodustades keeruka väga hargnenud kolmemõõtmelise struktuuri.
Siiani pole me sellele probleemile tähelepanu pööranud numbri kohta molekuli elementaarühikud, mis on vajalikud aine klassifitseerimiseks polümeer. Mis on see arv, mis moodustab partii mõiste?
Sellele küsimusele pole täpset vastust. Üldiselt vastab polümeerile suvaline arv kaks või enam. Kuid mitut ühikut sisaldavaid polümeere nimetatakse tavaliselt dimeerideks, trimeerideks, tetrameerideks jne vastavalt nende algsete molekulide ehk monomeerühikute arvule ja terminile. polümeer (täpsemalt, kõrge polümeer ) viitab juhtumile, kui ahelasse kuuluvate lülide arv on piisavalt suur. Kõrge polümeeri monomeeride minimaalne arv on umbes 100. Maksimaalne arv lingid teoreetiliselt piiramatud
2. Looduslikud polümeerid
2.1. kiudaineid
Tööstusliku tähtsusega looduslike polümeeride seas on kõige olulisem koht nii taimset kui loomset päritolu kiududel.
Kiu peamine omadus on selle kõrge tõmbetugevus. See spetsiifiline omadus on tingitud molekulide teatud paigutusest kiu struktuuris. Kiud sisaldavad tavaliselt väga väikeseid kristalle ja kristalliite ning need kristallidid on piki kiudu piklikud või "orienteeritud" nii, et pika ahelaga molekulid on paralleelsed või peaaegu paralleelsed kiu teljega. Selline kettide geomeetriline paigutus takistab kõige tõhusamalt konstruktsiooni deformeerumist või hävimist tõmbejõudude mõjul.
Hangi täistekstAlates iidsetest aegadest on laialdaselt kasutatud looduslikke kiude, mis põhinevad keemilisel ainel - tselluloosil. Tal on üsna keeruline struktuur ahel, mille korduvaks lüliks on ühend C6H10O5.
Teised tööstuslikult olulised looduslikud kiud on vill ja siid. Need on loomse päritoluga tooted. Siidiusside näärmed eritavad siidikiude, millest moodustub kookon. Keemilisest vaatenurgast on vill ja siid valgud, väga suur ainete klass, mis on taimede ja loomade maailmas laialt levinud.
Valgud erinevad juba käsitletud polümeeridest selle poolest, et nende ahel on üles ehitatud ebavõrdse keemilise struktuuriga korduvatest elementidest. Üldvalem valguahela elementaarne lüli
Helistage" href="/text/category/koll/" rel="bookmark">kollageenile, peamisele nahavalgule.
Naha tugevus, mis saavutatakse nahkade keemilise töötlemisega (parkimisega), tuleneb neid moodustavast kollageenkiudude võrgustikust.
3. Sünteetilised polümeerid
3.1. kiudaineid
Kiudude hulgas tuleb eristada sünteetilisi, st neid, mille suured molekulid on ehitatud või sünteesitud väga lihtsatest keemilistest ühenditest ja looduslikest polümeeridest (tavaliselt tselluloosist) saadud keemilise töötlemise teel muudesse vormidesse. Mõlemad seda tüüpi polümeerid on kombineeritud üldnimetuse all keemilised kiud . Pideva niitkiu tootmiseks peab lähtepolümeer olema vedel – sula või lahuse kujul. Tselluloosil kui võimalikul materjalil sellistel eesmärkidel on suur puudus - see mitte ainult ei sula, vaid ei lahustu ka vees ega tavalistes orgaanilistes lahustites. Seetõttu tuleb tselluloosi kasutamiseks seda töödelda. Üks töötlemismeetodeid on tselluloosi mõjutamine äädikhape, mille tulemusena muundatakse tselluloosatsetaadiks. Tselluloosatsetaat lahustub hästi orgaanilistes lahustites, nagu atsetoon; see moodustab väga viskoosse siirupise lahuse, mille saab suruda läbi mitme kanaliga tsentrifuugi, mis sisaldab vajalik number väikesed augud; selle tulemusena saadakse kimp peeneid kiude, mis pärast lahusti tõmbamist ja aurustamist moodustavad pideva tselluloosatsetaadi niidi. Teist tüüpi ekstrudeeritud vedelas massis töödeldakse keemiliselt modifitseeritud tselluloosi, muutes selle algseks tselluloosiks. See viskoossiidina tuntud toode on näide regenereeritud tsellulooskiust.
Kõik sünteetilised polümeerkiud on toodetud pidevate filamentide kujul. Erinevalt tselluloosist saab neid polümeere kergesti sulatada.
Sünteetilisi kiude ei tohiks käsitada looduslike kiudude asendajatena ega kunstkiududena; neil on erinevad omadused ja nad on mõnes mõttes paremad kui looduslikud kiud. Sünteetilisi kiude on mitut tüüpi: nailonid, polüestrid (terüleen, lavsan), akrüülkiud (orlon) ja polüpropüleenkiud (alstron).
3.2. Kummikud
Bunakumm oli enne II maailmasõda kõige olulisem sünteetiline kautšuk: butadieen on ahela korduv lüli.
Aafrikas otsiti erinevaid kummitaimi ja kuigi soovitud taimi leiti mitmeid, osutus nende potentsiaalne panus tähtsusetuks. Olukorda leevendas Ameerika sünteetilise kummi, tuntud kui GR-S, tulek.
Sellel on keerulisem struktuur kui Saksa buna kummil, see on kopolümeer, mis koosneb kahest komponendist - butadieenist ja stüreenist. See kumm osutus mitmete omaduste poolest looduslikust kummist halvemaks, selle ebapiisav “kleepuvus” ehk nakkuvus tekitas raskusi näiteks autorehvide tootmisel, kuid see probleem lahenes pärast segamistehnoloogiate väljatöötamist. see koos väikesed kogused looduslik kautšuk.
Hangi täistekstTeine oluline sünteetiline kautšuk on butüülkummi, isobutüleenist saadud polümeer. Butüülkummi üks omadusi on aga see, et õhk difundeerub sellest läbi palju aeglasemalt kui läbi loodusliku kummi, mistõttu on butüülkummi väärtuslik alus autode sisekummide tootmisel. Kuid võrreldes loodusliku kummiga on selle elastsed omadused palju halvemad.
Erinevalt kiududest ei ole kummid üldiselt kristalsed; nende molekulid on juhuslikult paigutatud. Kummide struktuuri, mis on paljuski sarnane vedeliku struktuuriga, nimetatakse amorfseks. Just sellele lahtisele struktuurile (erinevalt tihedalt pakitud korrapärasele kristallstruktuurile) võlgnevad kummid oma pehmuse ja paindlikkuse.
3.3. Kristallilised polümeerid
Kolmas ja paljuski kõige huvitavam sünteetiliste polümeeride klass on kristalsed polümeerid. Erinevalt tavalisest kristallilisest tahked ained polümeerid ei ole täielikult kristalsed, vaid sisaldavad palju väga väikeseid kristalle, mis eksisteerivad koos ülejäänud korrastamata või amorfse ainega. Orienteerimata olekus pole neil looduses analooge ning nende omadused erinevad seni teadaolevate ainete omadest.
Üks levinumaid ja mitmekülgsemaid kristallilisi polümeere on polüetüleen. Sellel on suurepärased isoleerivad omadused, samuti kergus ja elastsus. Polüetüleenil on üks puudus – OH sulab suhteliselt madalal temperatuuril (110°C-130°C)
Teine oluline kristalne polümeer on nailon, millel on suurepärased kiudu moodustavad omadused, kuid millest saab valmistada ka survevalu plokke. Tpl. (nailon) - 265°С.
Polümeerses heteroahelalises struktuuris on boorhüdriid
/text/categ/nauka.php" class="myButtonNauka">Hangi täistekst

Organoelementpolümeerid sisaldavad nii orgaanilisi kui anorgaanilisi rühmi. Heteroahelalise organoelemendi polümeeri näiteks on polüdimetüülsiloksaan [-Si(CH3)2O-]n. Või näiteks polüorganofosfaseenid[-PR2=N-]n.
Nimetatakse polümeere, mille makromolekulid koosnevad sama tüüpi korduvatest ühikutest homopolümeerid . AT kopolümeerid makromolekulid sisaldavad mitut tüüpi monomeerühikuid. Järgmine on kopolümeeride klassifikatsioon, mis sisaldavad kahte tüüpi korduvaid ühikuid, mida tavaliselt tähistatakse kui A ja B:
Põhiahela ehituse seisukohalt jagunevad makromolekulid lineaarseteks, kaheahelalisteks (kaks paralleelset ahelat on mitmel viisil seotud), hargnenud ja ristseotud (võrk). Järgmine on makromolekulide klassifikatsioon põhiahela struktuuri järgi:
Konfiguratsiooni tüüp | Keti struktuur |
Lineaarsed makromolekulid | |
Kaheahelalised makromolekulid trepp spiropolümeerid | |
Hargnenud makromolekulid | |
statistiline | |
kammikujuline | |
tähtkuju | |
Õmmeldud (võrk) | |
tasapinnas (parkett) | |
kosmoses |
7. Termilised üleminekud polümeerides
Polümeeride puhul on kahte peamist üleminekutemperatuuri tüüpi: sulamistemperatuur (Tm.) ja klaasistumistemperatuur (Tst.).
Sulamistemperatuur on polümeeri kristalse faasi sulamistemperatuur.
Klaasistumistemperatuur on temperatuur, mille juures polümeeri amorfsed piirkonnad omandavad klaasjas olekule iseloomulikud omadused: rabedus, jäikus ja tugevus. Nende kahe termilise ülemineku erinevusi saab hõlpsasti mõista, võttes arvesse muutusi, mis toimuvad erinevas vedelas polümeeris selle jahutamisel. Temperatuuri langedes väheneb translatsiooni-, pöörlemis- ja vibratsioonienergia polümeeri molekulis. Kui molekuli koguenergia väheneb väärtuseni, mille juures translatsiooni- ja pöörlemisenergia praktiliselt puuduvad, muutub polümeeri kristalliseerumine võimalikuks. Veelgi enam, kui teatud sümmeetrianõuded on täidetud, võivad molekulid olla järjestatud paigutusega ja seega toimub kristalliseerumine. Temperatuur, mille juures see protsess toimub, on Tpl.. Kuid mitte kõik polümeerid ei loo vajalikud tingimused kristalliseerimiseks. Kui sümmeetrianõuded ei ole täidetud, siis kristalliseerumine ei toimu, kuid kui temperatuur veelgi langeb, väheneb molekuli energia edasi. Jõudes Tst. polümeeri ahelate segmentaalne liikumine peatub sidemete pöörlemise tugeva nõrgenemise tõttu.
See, kas võib toimuda üks või mõlemad termilised üleminekud, sõltub selle morfoloogiast. Täiesti amorfseid polümeere iseloomustavad ainult Tst., samas kui polümeeridel on täiskristallilistel polümeeridel ainult Tpl.. Enamik polümeere Tpl. läbivad ainult osaliselt kristalliseerumise, selliseid poolkristallilisi polümeere iseloomustab sulamistemperatuur ja klaasistumistemperatuur. Termilisi üleminekuid on lihtne mõõta, muutes selliseid omadusi nagu erimaht, soojusmahtuvus. Joonisel on kujutatud erimahu sõltuvust temperatuurist täiesti amorfse ja täiesti kristalse polümeeri puhul (pidevad jooned). Sulamistemperatuur on see esimest järku üleminek väga järsu erimahu muutusega; klaasi moodustumise temperatuur on teist järku üleminek, mida iseloomustab ainult konkreetse ruumala temperatuurikoefitsiendi muutus. Poolkristallilise polümeeri vastav kõver koosneb kristalse polümeeri kõverast ja punktiirjoonest, mis vastab üleminekupiirkonnale klaasjas olekusse.

Riis. 2. Polümeeri klaasistumistemperatuuri ja sulamistemperatuuri määramine selle erimahu muutmise teel.
Polümeeri sulamis- ja klaasistumistemperatuurid mõjutavad polümeeri mehaanilisi omadusi antud temperatuuril ja määravad ära selle kasutamise temperatuurivahemiku. Mõlemat termilist üleminekut mõjutavad reeglina võrdselt molekulaarne sümmeetria, struktuurne jäikus ja molekulidevaheline interaktsioon. Tugev molekulidevaheline interaktsioon (kõrge polaarsuse või vesiniksidemed). Tst. on kõrged väärtused.
Summa järgi Tst. ja Tm. polümeeri ahelate molekulaarne sümmeetria mõjutab samuti tugevalt. Struktuuriliselt asümmeetrilistel polümeeridel (nagu polüvinüülkloriid ja polüpropüleen) on kõrgem Tst. ja Tpl., kui nende sümmeetrilised analoogid (polüvinülideenkloriid ja polüisobutüleen). Asümmeetrilised ahelad on polaarsemad ja võivad seetõttu tihedamalt pakkida, pakkudes tugevamat molekulidevahelist interaktsiooni.
8. Valgud
Valgud on polümeerid, täpsemalt kopolümeerid, mis koosnevad aminohappejääkidest, mis erinevad R-radikaali olemuse poolest.
Hangi täistekstNeid nimetatakse biopolümeerideks:
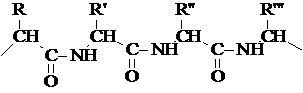
Valkude koostis sisaldab 20 kõige universaalsemat, nn "maagilist" aminohapet ja kuni kümmekond haruldasemat. Erinevate valkude makromolekulides vahelduvad need aminohapped erineval viisil. Mõnede valkainete keemiline struktuur on dešifreeritud, kuid selliste ainete nagu kaseiin, keratiinid, kollageen, mida kasutatakse tööstuses, valemid on teadmata.
Kaseiin- kompleksvalk, mis moodustub kaseinogeenist (piima, kodujuustu ja juustu kõige olulisem komponent) selle hüübimise käigus ensüümide toimel. Lisaks C, H, O ja N aatomitele sisaldab kaseiin P.
Keratiinid- valgulised ained, mis on peamised lahutamatu osa kuded, mis täidavad loomorganismides katte- ja kaitsefunktsioone (nahk, sarv, karv, vill). Keratiinid on iseloomustatud kõrge sisaldus väävel.
Kollageen - valguline aine, komponent sidekoe; eriti palju kollageeni leidub loomade luudes.
Loomade luude, sarvede ja naha spetsiaalsel töötlemisel tööstuses saadakse želatiin - loomse päritoluga valkainete segu.
Valgud on molekulaarsed tööriistad, mille abil realiseeritakse geneetilist teavet.
See on DNA nukleotiidide lineaarses järjestuses sisalduv teave, mis määrab sünteesitud valgu polüpeptiidahela aminohapete lineaarse järjestuse. Saadud lineaarne polüpeptiidahel ise on nüüd varustatud funktsionaalse teabega, mille kohaselt see muundub spontaanselt teatud stabiilseks kolmemõõtmeliseks struktuuriks. Seega volditakse labiilne polüpeptiidahel kokku, keeratakse valgu molekuli ruumistruktuuri ja mitte juhuslikult, vaid rangelt kooskõlas aminohappejärjestuses sisalduva teabega.
9. Keemilised sidemed valgu molekulis
Üldiselt iseloomustab valgu molekuli tugevate kovalentsete ja suhteliselt nõrkade mittekovalentsete sidemete olemasolu. Selline sidemete kombinatsioon annab valkudele teatud tugevuse ja dünaamilisuse oma toimimisprotsessis.

Riis. 3. Keemilised sidemed valgu molekulis.
Joonisel on kujutatud valgu molekulis olevate aminohappejääkide radikaalide vaheliste sidemete tüübid.
a) elektrostaatiline interaktsioon
b) vesiniksidemed
c) mittepolaarsete külgahelate vastastikmõju, mis on põhjustatud hüdrofoobsete radikaalide väljutamisest lahusti molekulide poolt "kuiva" tsooni.
d) disulfiidsidemed (kahekordne kõverjoon tähendab polüpeptiidsideme selgroogu)
kovalentsed sidemed valgu molekulis võib olla kahte tüüpi - disulfiid ja peptiid.
Peptiid ehk happeamiid (-CO-NH-) tekib ühe aminohappe karboksüülrühma ja teise a-aminorühma interaktsioonist.
Röntgendifraktsioonianalüüsi kasutades leiti, et peptiidüksuse karbonüülaatomi ja lämmastikuaatomi vaheline side on osaliselt kaksikside.
Sideme pikkus » 0,132 nm, mis on keskmine nende aatomite vahelistele kaksiks- ja üksiksidemetele vastavate kauguste vahel. Side - CO-NH - on trans-konfiguratsiooniga ja naaber-a-süsiniku aatomid on trans-asendis. Trans-peptiidrühm on jäik ja vaba pöörlemine on võimalik ainult C-C ja N-Ca sidemete ümber. Nende sidemete ümber pöörlemist iseloomustavad erinevad nurgad.
Valgumolekuli ruumilise struktuuri stabiliseerimisel mängivad olulist rolli kovalentsed disulfiidsidemed (S-S), mis tekivad tsüsteiinijäägi sulfhüdrüülrühmade oksüdatsiooni tulemusena.
Mittekovalentsed sidemed ja interaktsioonid mängivad olulist rolli valgumolekuli konformatsiooni stabiliseerimisel. Nende hulka kuuluvad hüdrofoobsed interaktsioonid, elektrostaatilised, ioonsed ja vesiniksidemed.
Hüdrofoobne interaktsioon tekib siis, kui mõne aminohappe hüdrofoobsed süsivesinikud ja aromaatsed radikaalid lähenevad üksteisele. Hüdrofoobse interaktsiooni protsessi võib kujutada kui polüpeptiidahela mittepolaarsete rühmade liikumist veest hüdrofoobsetesse piirkondadesse.
Vesiniksidemed moodustuvad vesinikuaatomite vahel, mis on kovalentselt seotud aatomiga, mis sisaldab jagamata elektronpaari, ja teise elektronegatiivse aatomi (N või O) vahel. Valkudes ja polüpeptiidides võivad vesiniksidemed olla ahelasisesed ja ahelatevahelised. Ahelisisesed vesiniksidemed stabiliseerivad a-spiraalseid ja ahelatevahelised b-lehtedega struktuure.
Ioonsed (soola) sidemed moodustuvad monoaminodikarboksüülaminohapete dissotsieerunud vabadest karboksüülrühmadest (COO-) ja diaminomonokarboksüülaminohapete protoneeritud vabadest aminorühmadest (NH3+). Ioonsed sidemed võivad olla ahelasisesed ja ahelatevahelised.
10. Valgu molekuli struktuurse organiseerituse tasemed
Valkude funktsionaalsed omadused määratakse aminohappejärjestuse ja konfiguratsiooniga, st nende struktuurse korralduse või ruumilise struktuuriga. Sellest vaatenurgast eristatakse nelja tasandit: esmane, sekundaarne, tertsiaarne ja kvaternaarne struktuur.
10.1. Esmane struktuur
Nad mõistavad aminohapete kvalitatiivset ja kvantitatiivset koostist, samuti nende järjestust valgu molekuli polüpeptiidahelates. alus esmane struktuur moodustavad peptiidsidemeid.
Hangi täistekstPrimaarstruktuuri andmete analüüs võimaldab teha järgmised järeldused:
1. Primaarstruktuuri stabiilsuse tagavad peamiselt peamised valentsed peptiidsidemed; Võimalik osalemine ja väike arv disulfiidsidemed.
2. Polüpeptiidahelas võib leida erinevaid aminohapete kombinatsioone; korduvad järjestused on polüpeptiidides suhteliselt haruldased.
3. Iga üksikut homogeenset valku iseloomustab ainulaadne esmane struktuur; aminohapete asendamise sagedus ei too kaasa mitte ainult struktuurseid ümberkorraldusi, vaid ka muutusi füüsilised ja keemilised omadused ja bioloogilised funktsioonid.
4. Mõnedes sarnaste omadustega ensüümides leitakse identseid peptiidstruktuure, eriti nende aktiivsete keskuste piirkondades.

Riis. 4. RNaasi esmane struktuur. (neli disulfiidsidet esile tõstetud).
http://pandia.ru/text/78/042/images/image035_7.jpg" width="324" height="344 src=">
Riis. 6. a-spiraalne a) a-peptiidi konfiguratsiooniga polüpeptiidahel; b) spiraali skelett.
10.2.2. b-volditud struktuur
Aminohappejärjestuse sellise ruumilise paigutusega moodustub paralleelselt ja antiparalleelselt paigutatud ühe või mitme polüpeptiidahela fragmentide süsteem. B-voltide polüpeptiidahelad on täielikult pikendatud.

Joonis 7. b-volditud struktuur a) külgvaade; b) pealtvaade.
Voldid ilmuvad tänu sellele, et kahe kõrvuti asetsevad lennukid peptiidsidemed moodustavad mingi nurga. Süsteemi stabiliseerivad ristseotud vesiniksidemed ahelate vahel, mis on risti peptiidsidemete orientatsiooniga.
Kiudude vaheline kaugus on 0,95 nm ja identsuse periood piki ahelat on paralleelsete ahelate puhul 0,70 nm ja antiparalleelsete ahelate puhul 0,65 nm.
10.2.3. Kollageeni spiraal
See koosneb kolmest spiraalsest tropokollageenist, mis on varda kujulised, läbimõõduga 1,5 nm ja pikkusega umbes 300 nm. Spiraalketid keerduvad üksteise ümber ja moodustavad superspiraali. Kahe aminohappejäägi vaheline kaugus piki heeliksi telge on 0,29 nm. Kollageeni heeliksit stabiliseerivad vesiniksidemed, mis tekivad ühe ahela aminohappejääkide peptiidi NH-rühmade vesiniku ja teise aminohappejääkide CO-rühmade hapniku vahel. See struktuur annab kollageenile elastsuse ja tugevuse.
10.2.4. Supersekundaarsed struktuurid ja struktuurivaldkonnad
Röntgendifraktsioonianalüüsi meetoditega on nüüd tõestatud veel kahe valgu molekuli struktuurse organiseerituse taseme olemasolu, mis osutusid sekundaarsete ja tertsiaarsete struktuuride vahepealseks. Need on nn suprasekundaarsed struktuurid ja struktuurivaldkonnad. Esimesed on polüpeptiidahelate agregaadid, millel on oma sekundaarne struktuur ja mis moodustuvad osades valkudes nende termodünaamilise või kineetilise stabiilsuse tulemusena.
10.3. Tertsiaarne struktuur
Tertsiaarse struktuuri all mõeldakse polüpeptiidheeliksi ruumilist orientatsiooni või meetodit polüpeptiidahela paigutamiseks teatud mahus.
Esimene valk, mille tertsiaarstruktuuri selgitas J. Kendrew röntgendifraktsioonanalüüsi põhjal, oli kašelotti müoglobiin.
http://pandia.ru/text/78/042/images/image038_4.jpg" width="389" height="239">
Riis. 9. Tertsiaarstruktuuri stabiliseerivate mittekovalentsete sidemete tüübid.
a) elektrostaatiline interaktsioon; b) vesinikside; c) mittepolaarsete rühmade hüdrofoobsed interaktsioonid; d) dipool-dipool vastastikmõju; e) disulfiid (kovalentne) side
Valgu tertsiaarne struktuur moodustub pärast sünteesi lõppu ribosoomides automaatselt ja selle määrab täielikult esmane struktuur.
Seega on polüpeptiidahela lineaarne ühemõõtmeline struktuur varustatud erinevat tüüpi - konformatsioonilise - teabega, mis määrab kindla kujuga valgu molekuli moodustumise teatud kindla kujuga. ruumiline paigutus. Valgumolekuli kolmemõõtmeline struktuur omakorda sisaldab ka informatsiooni, kuid hoopis teist tüüpi, nimelt funktsionaalset informatsiooni, mida muidu nimetatakse molekulisiseseks informatsiooniks.
10.4. Kvaternaarne struktuur
See mõiste tähendab iseloomulikku viisi üksikute polüpeptiidahelate kombineerimiseks ja ruumis paigutamiseks, mis moodustavad ühe funktsionaalselt individuaalse molekuli.
Kvaternaarse struktuuri moodustamisel osalevad vesiniksidemed, elektrostaatilised, van der Waalsi ja hüdrofoobsed vastasmõjud.
Mõnede valkude kvaternaarset struktuuri iseloomustab alaühikute globulaarne paigutus (hemoglobiin), teised valgud on ühendatud spiraalseteks kvaternaarseteks struktuurideks nagu spiraalne mosaiik (tubaka mosaiikviirus)
Järeldus
Seega on valgumolekuli struktuuris neli taset. Kõik struktuuritasemed on omavahel seotud ja aminohappejääkide järjestus ehk primaarstruktuur määrab täielikult valgumolekuli konformatsiooni. Bioloogilise aktiivsuse ilming sõltub kõrgemad tasemed nende struktuurne korraldus.
Kirjandus
1. et al. Sissejuhatus polümeeride keemiasse: Õpetus ped jaoks. Ülikoolid / jne M., Kõrgem. kool, 1988
2. J. Oudian. Polümeeride keemia alused. Per. inglise keelest. . Ed. vastav liige NSVL Teaduste Akadeemia V. V. Kormak. Ed. Mir, Moskva, 1974
3. A. Trilor. Sissejuhatus polümeeriteadusesse. Per. inglise keelest. Ed. Mir, Moskva, 1973
4. Perepetšenko polümeeride füüsikasse.-M., "Keemia", 1978
5. Polümeeride kormaki struktuur ja temperatuuriomadused. "Teadus", 1970
6. Polümeerist sildistaja
7. Makromolekulaarsed ühendid: õpik ülikoolidele. – 3. väljaanne, Higher. kool, 1981. -656s.
8. Kutšerenko: õpik / N. E Kucherenko ja teised - K: Vyscha kool, Kiievi ülikooli kirjastus, 1988
9., Korovini keemia: õpik, toim. .- M.: Meditsiin, 1983
Valgud on looduslikud polümeerid, mis koosnevad peptiidsidemetega seotud alfa-aminohappe jääkidest. Valgud on osa kõigi elusorganismide rakkudest ja kudedest. Nad osalevad elu kõige olulisemates protsessides organism- vahetus ained, paljunemine, kehakasv, lihastöö jne. Need on meie toidu põhikomponent.
Uuringu ajalugu Valgud on isoleeritud aastal eraldi klass bioloogilised molekulid 18. sajandil prantsuse keemiku Antoine Fourcroix’ töö tulemusena. Hollandi keemik Gerrit Mulder analüüsis valkude koostist ja püstitas hüpoteesi, et peaaegu kõigil valkudel on sarnane empiiriline valem. Mõiste "valk" selliste molekulide jaoks pakkus 1838. aastal välja Rootsi keemik Jakob Berzelius. Mulder määras ka aminohapete valkude lagunemissaadused ja ühele neist (leutsiin) määras väikese veamääraga molekulmassi 131 daltonit. Aastal 1836 pakkus Mulder välja esimese valkude keemilise struktuuri mudeli. Lähtudes radikaalide teooriast, sõnastas ta miinimumi mõiste struktuuriüksus valgu koostis, C16H24N4O5, mida nimetati "valguks", ja teooria "valguteooria" Hollandi keemik Gerrit Mulder analüüsis valkude koostist ja püstitas hüpoteesi, et peaaegu kõigil valkudel on sarnane empiiriline valem. Mõiste "valk" selliste molekulide jaoks pakkus 1838. aastal välja Rootsi keemik Jakob Berzelius. Mulder määras ka aminohapete valkude lagunemissaadused ja ühele neist (leutsiin) määras väikese veamääraga molekulmassi 131 daltonit. Aastal 1836 pakkus Mulder välja esimese valkude keemilise struktuuri mudeli. Radikaalide teooriale tuginedes sõnastas ta valgu koostise minimaalse struktuuriüksuse C16H24N4O5 mõiste, mida nimetati "valguks" ja teooria "valguteooria"

Valkude struktuur Saksa keemik Emil Fischer pakkus välja, et valgud on peptiidsidemetega seotud aminohapete polümeerid. Valkude struktuuri polümeerse olemuse ideed, nagu hästi teada, väljendasid Danilevsky ja Hert, kuid nad uskusid, et "monomeerid" on väga keerulised moodustised - peptoonid või "süsinik-lämmastiku kompleksid". Aminohappejääkide ühendi peptiiditüübi tõestamine. E. Fisher lähtus järgmistest tähelepanekutest. Esiteks tekkisid nii valkude hüdrolüüsil kui ka nende ensümaatilisel lagunemisel erinevad aminohapped. Teisi ühendeid oli äärmiselt raske kirjeldada ja veelgi raskem saada. Lisaks teadis Fischer, et valkudel ei ole ülekaalus ei happelisi ega aluselisi omadusi, mis tähendab, et aminohapete koostises olevad amino- ja karboksüülrühmad valgumolekulides on suletud ja justkui varjavad üksteist. Töö edukas elluviimine viis Fisheri eduni. Selle kallal töötades oli ta juba aastatel paralleelselt. Ta tõestas esimest korda, et valkude koostises on ainult aminohapete L-stereoisomeerid. peptiidside
![]()

Valgu struktuurid Esmane struktuur Primaarne struktuur on aminohapete järjestus polüpeptiidahelas. Olulised omadused esmane struktuur on mängivate aminohapete kombinatsiooni konservatiivsed motiivid võtmeroll valgu funktsioonides. Liigi evolutsiooni käigus säilivad konservatiivsed motiivid, mis võimaldavad sageli ennustada tundmatu valgu funktsiooni. evolutsiooni konservatiivsed motiivid Esmastruktuur evolutsiooni konservatiivsed motiivid

Sekundaarne struktuur Polüpeptiidahela fragmendi lokaalne järjestamine, stabiliseeritud vesiniksidemetega. vesiniksidemed vesiniksidemed Valkude sekundaarstruktuuri tüübid: - α-heeliksid;α-heeliksid - β-lehed (volditud kihid);β-lehed volditud kihid - π-heeliksid; - 3-heeliks; - järjestamata killud. Valgu sekundaarne struktuur

Tertsiaarne struktuur ruumiline struktuur polüpeptiidahel (valgu moodustavate aatomite ruumiliste koordinaatide kogum). Struktuurselt koosneb sekundaarstruktuuri elementidest, stabiliseeritud erinevat tüüpi interaktsioonid, milles mängivad hüdrofoobsed vastasmõjud oluline roll. Tertsiaarse struktuuri stabiliseerimisel osalevad: kovalentsed sidemed (disulfiidsillad kahe tsüsteiinijäägi vahel); kovalentsed sidemed (disulfiidsillad kahe tsüsteiinijäägi vahel); ioonsed sidemed aminohappejääkide vastaslaenguga külgrühmade vahel; ioonsidemed aminohappejääkide vastaslaenguga külgrühmade vahel; vesiniksidemed; vesiniksidemed; hüdrofiilsed-hüdrofoobsed interaktsioonid. hüdrofiilsed-hüdrofoobsed interaktsioonid.

Kvaternaarne struktuur (või allüksus, domeen) vastastikune kokkulepe mitu polüpeptiidahelat ühe valgukompleksi osana. valgu molekulid, mis on osa kvaternaarse struktuuriga valgust, moodustuvad ribosoomidel eraldi ja alles pärast sünteesi lõppu moodustavad ühise supramolekulaarse struktuuri. Kvaternaarse struktuuriga valk võib sisaldada nii identseid kui ka erinevaid polüpeptiidahelaid. Kvaternaarse struktuuri stabiliseerimisel osalevad samad interaktsioonitüübid kui tertsiaarstruktuuri stabiliseerimisel. Supramolekulaarsed valgukompleksid võivad koosneda kümnetest molekulidest.


Fibrillaarsed valgud on pikliku niitja struktuuriga valgud, mille risttelje ja pikitelje suhe on suurem kui 1:10. Enamik fibrillaarseid valke on vees lahustumatud, suure molekulmassiga ja väga korrapärase ruumilise struktuuriga, mida stabiliseerivad peamiselt interaktsioonid (ka kovalentsed) erinevate polüpeptiidahelate vahel. Esmane ja sekundaarne struktuur fibrillaarne valk on samuti tavaliselt korrapärane. pikliku filamentse struktuuriga valgud, mille risttelje ja pikitelje suhe on suurem kui 1:10. Enamik fibrillaarseid valke on vees lahustumatud, suure molekulmassiga ja väga korrapärase ruumilise struktuuriga, mida stabiliseerivad peamiselt interaktsioonid (ka kovalentsed) erinevate polüpeptiidahelate vahel. Ka fibrillaarse valgu primaarne ja sekundaarne struktuur on tavaliselt korrapärane.

Globulaarsed valgud on valgud, mille molekulides polüpeptiidahelad tihedalt volditud kompaktseteks sfäärilisteks kerakujulisteks struktuurideks (tertsiaarsed valgustruktuurid). valgud, mille molekulides on polüpeptiidahelad tihedalt volditud kompaktseteks sfäärilisteks kerakujulisteks struktuurideks (tertsiaarseteks valgustruktuurideks). Globulaarsete valkude hulka kuuluvad ensüümid, immunoglobuliinid, mõned valgulised hormoonid (näiteks insuliin), aga ka muud valgud, mis täidavad transpordi-, reguleerimis- ja abifunktsioone.

Keemilised omadused Denaturatsioon on antud valgu molekulile omase ruumilise struktuuri osaline või täielik hävitamine. Võib olla pöörduv või pöördumatu. Denaturatsioon toimub järgmistel juhtudel: Denaturatsioon – antud valgu molekulile omase ruumilise struktuuri osaline või täielik hävitamine. Võib olla pöörduv või pöördumatu. Denatureerimine toimub: - kõrge temperatuuri - kõrge temperatuuri - hapete, leeliste ja kontsentreeritud soolalahuste - hapete, leeliste ja kontsentreeritud soolalahuste - raskmetallide soolade lahuste - raskmetallide soolade lahuste - mõne mõju all. orgaaniline aine(formaldehüüd, fenool) - mõned orgaanilised ained (formaldehüüd, fenool) - radioaktiivne kiirgus - radioaktiivne kiirgus

Värvusreaktsioonid Biureetreaktsioon – uurea kuumutamisel moodustub biureet, mis vasksulfaadi lahusega leelise juuresolekul annab violetse värvuse. Biureedi reaktsiooni annavad amiidrühma sisaldavad ained ja see rühm esineb valgu molekulis.



Valgu funktsioonid Struktuurne funktsioon; Struktuurne funktsioon; Kaitsefunktsioon; Kaitsefunktsioon; Reguleeriv funktsioon; Reguleeriv funktsioon; Signaali funktsioon; Signaali funktsioon; transpordifunktsioon; transpordifunktsioon; Varu (varu) funktsioon; Varu (varu) funktsioon; Retseptori funktsioon; Retseptori funktsioon; Mootori (mootori) funktsioon. Mootori (mootori) funktsioon.


Abstraktne koostatud
Õpilane 10 "A" klass
Pavelchuk Vladislav
SISUSissejuhatus
1. Valkude struktuur.
2. Valkude klassifikatsioon.
3. Struktuurne korraldus valgu molekulid.
4. Valkude eraldamine.
5. Valkude värvireaktsioonid.
6. Valgu esmase struktuuri dešifreerimine.
7. Valkude funktsioonid.
8. Kuidas sünteesitakse valku.
9. Järeldus.
Bibliograafia
SISSEJUHATUS
Valgud koos nukleiinhapete, lipiidide, süsivesikute, mõnede madalmolekulaarsete orgaaniliste ainetega, mineraalsoolade ja veega moodustavad kõigi maismaaorganismide – loomsete ja taimsete, komplekssete ja elementaarsete – protoplasma. Mõiste "protoplasma" pakkus välja Tšehhi füsioloog Purkyne (1839), et tähistada elusraku sisu. Valkude sisaldus protoplasmas on reeglina palju suurem kui kõigi selle teiste komponentide sisaldus (arvestamata vett). Enamasti moodustavad valgud kuni 75-80% rakkude kuivmassist.
Valguained esindavad protoplasma peamist, kõige aktiivsemat osa: „Protoplasmas on selle komponendi omadused, mis esinevad protoplasmas. rohkem ja mis on kõige aktiivsem "A. Ya. Danilevsky (protoplasma põhiaine ja selle modifitseerimine eluga. 1894).
Usk valkude esmatähtsusse eluks jääb vankumatuks ka meie ajal, vaatamata nukleiinhapete rolli avastamisele pärilikkusnähtustes, vitamiinide, hormoonide jm elutähtsuse selgitamisele. tegevust.
Oma koostise ja struktuuri iseärasuste tõttu on valkudel märkimisväärne hulk füüsikalisi ja keemilisi omadusi. On teada valgud, mis on vees täiesti lahustumatud, on valke, mis on äärmiselt ebastabiilsed, muutudes nähtava valguse või isegi kerge mehaanilise puudutuse mõjul. On valke, mille molekulid näevad välja nagu niidid, ulatudes mitme millimeetri pikkuseks, ja on valke, mille molekulid on mitmekümne angrammise läbimõõduga pallid. Kuid kõigil juhtudel on valkude struktuur ja omadused tihedas ja vastastikuses seoses nende funktsiooniga.
I. Valkude struktuur.
Valgud on raku kõige arvukam ja mitmekesisem orgaaniliste ühendite klass. Valgud on bioloogilised heteropolümeerid, mille monomeerideks on aminohapped. kõigil aminohapetel on vähemalt üks aminorühm (-NH2) ja karboksüülrühm (-COOH) ning need erinevad ®-radikaalide struktuursete ja füüsikalis-keemiliste omaduste poolest.
Peptiidid, mis sisaldavad mitut aminohappejääki kuni mitmekümneni, eksisteerivad kehas vabas vormis ja neil on kõrge bioloogiline aktiivsus. Nende hulka kuuluvad mitmed hormoonid (oksütotsiin, adrenokortikotroopne hormoon), mõned väga mürgised mürgised ained (näiteks seente amanitiin), aga ka paljud mikroorganismide poolt toodetud antibiootikumid.
Valgud on suure molekulmassiga polüpeptiidid, mis sisaldavad sada kuni mitu tuhat aminohapet.
II. VALGU KLASSIFIKATSIOON
Valgud jagunevad valkudeks (lihtvalgud), mis koosnevad ainult aminohappejääkidest, ja proteiidideks (kompleksvalgud), mis hüdrolüüsimisel annavad aminohappeid ja mittevalgulisi aineid (fosforhape, süsivesikud, heterotsüklilised ühendid, nukleiinhapped). Valgud ja proteiinid jagunevad mitmeks alarühmaks.
Valgud
Albumiinid - suhteliselt väikese molekulmassiga valgud, lahustuvad vees hästi. Need soolatakse vesilahustest välja ammooniumsulfaadi küllastunud lahusega, kuumutamisel koaguleeruvad (denatureerivad). Munavalge on tüüpiline albumiinide esindaja. Paljud neist saadakse kristallilises olekus.
Globuliinid on valgud, mis ei lahustu puhtas vees, kuid lahustuvad soojas 10% Nacl lahuses. Puhas globuliin saadakse soolalahuse lahjendamisel rohke veega. Globuliin - kõige levinumad valgud, on osa lihaskiududest, verest, piimast, munadest, köögiviljaseemnetest.
Proamiinid lahustuvad vees vähe. Lahustage 60-80% etüülalkoholi vesilahuses. Prolamiinide hüdrolüüs põhjustab suurel hulgal aminohape proliin. teraviljaseemnetele iseloomulik. Näiteks on gliadiin, nisugluteeni peamine valk.
Gluteliinid lahustuvad ainult 0,2% leelises. Leidub nisu, riisi, maisi seemnetes.
Protamiine leidub ainult kalapiimas. Need koosnevad 80% aluselistest aminohapetest, seega on need tugevad alused. Täiesti väävlivaba.
Skleroproteiinid on lahustumatud valgud, neil on filamentsed (fibrillaarsed) molekulid. Sisaldab väävlit. Nende hulka kuuluvad kollageen (kõhre, mõnede luude valgud), elastiin (kõõluste, sidekudede valgud), keratiin (karvade, sarvede, sõrade, naha ülemise kihi valgud), fibroiin (toorsiidist niitide valk).
Valgud. Kompleksvalgud jagatakse rühmadesse sõltuvalt nende mittevalgulise osa koostisest, mida nimetatakse proteesrühmaks. Komplekssete valkude valguosa nimetatakse apoproteiiniks.
Lipoproteiinid hüdrolüüsitakse lihtsateks valkudeks ja lipiidideks. Lipoproteiinid sisalduvad suurtes kogustes klorofülli terade koostises ja rakkude protoplasmas, bioloogilistes membraanides.
Glükoproteiinid – hüdrolüüsitakse lihtsateks valkudeks ja suure molekulmassiga süsivesikuteks. Vees ei lahustu, kuid lahustub lahjendatud leelistes. Sisaldub erinevates loomade limaskesta sekretsioonides, munavalges,
Kromoproteiinid – hüdrolüüsitakse lihtsateks valkudeks ja värvaineteks. Näiteks vere hemoglobiin laguneb valkglobiiniks ja rauda sisaldavaks kompleksseks lämmastikaluseks.
Nukleoproteiinid hüdrolüüsitakse lihtsateks valkudeks, tavaliselt protamiinideks või histoonideks, ja nukleiinhapeteks.
Fosfoproteiinid – sisaldavad fosforhapet. mängivad suur roll noore organismi toitumises. Kaseiin, piimavalk, on näiteks.
III. VALGU MOLEKULIDE STRUKTUURNE KORRALDUS
Kuna valgud koosnevad mitmekümnest polüpeptiidahelas ühendatud aminohappest, on rakul energeetiliselt kahjumlik hoida neid ahela kujul (nn voldimata kujul). Seetõttu läbivad valgud tihendamise, voltimise, mille tulemusena omandavad nad teatud ruumiline korraldus- ruumiline struktuur.
Valkude ruumilisel korraldusel on 4 taset.
Esmane struktuur on aminohapete järjestus polüpeptiidahela koostises ja selle määrab nukleotiidide järjestus seda valku kodeeriva DNA molekuli piirkonnas. Iga valgu esmane struktuur on ainulaadne ja määrab selle kuju, omadused ja funktsioonid.
Enamiku valkude sekundaarstruktuur on spiraalikujuline ja tekib vesiniksidemete moodustumisel polüpeptiidahela erinevate aminohappejääkide CO- ja NH-rühmade vahel.
Tertsiaarstruktuur on spiraali või gloobuli kujuga ja moodustub valgu molekuli keerulise ruumilise paigutuse tulemusena. Igal valgutüübil on spetsiifiline gloobulite valem. Tertsiaarse struktuuri tugevuse annavad erinevad sidemed, mis tekivad aminohapete radikaalide vahel (disulfiid, ioonne, hüdrofoobne).
Kvaternaarne struktuur on keeruline kompleks, mis ühendab mitut tertsiaarset struktuuri (näiteks hemoglobiini valk koosneb neljast gloobulist), mida hoiavad mittekovalentsed sidemed: ioonsed, vesiniku- ja hüdrofoobsed sidemed.
Natiivse valgu ruumilise vormi ja sellest tulenevalt ka omaduste ja bioloogilise aktiivsuse muutust nimetatakse denaturatsiooniks. Denaturatsioon võib olla pöörduv või pöördumatu. Esimesel juhul on kvaternaarne, tertsiaarne või sekundaarne struktuur häiritud ja võimalik on valgu struktuuri taastamise pöördprotsess - renaturatsioon, teisel juhul purunevad peptiidsidemed primaarstruktuuris. Denaturatsiooni põhjustavad keemilised mõjud, kõrge temperatuur (üle 45 kraadi C), kiirgus, kõrge rõhk jne.
V. VALGU TAASTAMINE
Valgud ekstraheeritakse looduslikust materjalist vee, soolade, leeliste, hapete, vee-alkoholi lahustega. Sel viisil saadud toode sisaldab tavaliselt märkimisväärses koguses lisandeid. Valgu edasiseks eraldamiseks ja puhastamiseks töödeldakse lahust sooladega (väljasoolamine), küllastatakse alkoholi või atsetooniga ja neutraliseeritakse. Sel juhul eraldatakse vastav valgufraktsioon. Muutumatul kujul on valku väga raske eraldada, selleks on vaja jälgida terve rida tingimused: madalad temperatuurid, keskkonna teatud reaktsioon jne.
Eraldatud ja puhastatud valgud on enamasti valge pulbrina või säilitavad oma loomuliku vormi (näiteks villa- ja siidivalgud).
Molekulide kuju järgi võib valgud jagada kahte rühma: fibrillaarsed ehk filamentsed ja kerakujulised ehk sfäärilised. Fibrillaarsed valgud täidavad reeglina struktuuri moodustavaid funktsioone. Nende omadused (tugevus, venitatavus) sõltuvad polüpeptiidahelate pakendamise viisist, seetõttu säilitavad valgud pärast eraldamist tavaliselt oma loomuliku kuju. Fibrillaarsete valkude näideteks on siidfibroiin, keratiinid, kollageenid.
Teise rühma kuuluvad enamik inimkehas sisalduvatest valkudest. Globulaarseid valke iseloomustab kõrge reaktsioonivõimega saitide olemasolu (need võivad olla ensüümide katalüütilised keskused) või moodustavad komplekse teiste molekulidega ruumis üksteisele lähedal asuvate funktsionaalrühmade tõttu.
VI. VALGIDE VÄRVIREAKTSIOONID
Valke iseloomustavad mõned värvireaktsioonid, mis on seotud teatud rühmade ja aminohappejääkide olemasoluga nende molekulis.
Biureetreaktsioon - violetse värvuse ilmumine, kui valku töödeldakse leelise kontsentreeritud lahusega ja CuSO4 küllastunud lahusega. Seotud peptiidsidemete olemasoluga molekulis.
Ksantoproteiini reaktsioon - kollase värvuse ilmumine kontsentreeritud lämmastikhappe toimel valkudele. Reaktsioon on seotud aromaatsete tsüklite esinemisega valgus.
Miljoni reaktsioon - kirsipunase värvuse ilmumine valgu Milloni reagendiga (elavhõbenitraadi lahus dilämmastikhappes) kokkupuutel. Reaktsiooni seletatakse fenoolrühmade olemasoluga valgus.
Sulfhüdrüülreaktsioon - pliisulfiidi musta sademe sadestumine, kui valku kuumutatakse plussbitilahusega (valgus sisalduvate sulfhüdrüülrühmade tõttu).
Adamkevitši reaktsioon on lilla värvuse ilmumine, kui valgule lisatakse glüoksaal- ja kontsentreeritud väävelhapet. Seotud indoolirühmade olemasoluga.
VII. VALGU ESMASTRUKTUURI DEKOODEERIMINE
Valgu primaarstruktuuri dešifreerimine tähendab selle valemi kindlaksmääramist, st kindlaks teha, millises järjestuses aminohappejäägid polüpeptiidahelas asuvad.
Valgu esmase struktuuri tundmist illustreerivad hästi Ingrami töö andmed, mis uurisid mõnes Aafrikas ja Vahemere piirkonnas levinud päriliku verehaiguse, nn sirbikujulise aneemia põhjuseid. Sirpaneemiaga patsiendid on kahvatud, kurdavad nõrkust, õhupuudust vähimagi pingutuse korral. Nad elavad harva 12-17-aastaseks. Vereanalüüs näitab punaste vereliblede ebatavalist kuju. Patsientide erütrotsüüdid on poolkuu või poolkuu välimusega, normaalsed erütrotsüüdid aga kaksiknõgusate ketaste kuju. Üksikasjalik uuring näitas, et tervetes erütrotsüütides jaotub hemoglobiin ühtlaselt ja juhuslikult kogu rakus, samas kui aneemiliste patsientide erütrotsüütides moodustab hemoglobiin korrapäraseid kristallstruktuure. Hemoglobiini kristalliseerumise tõttu deformeeruvad erütrotsüüdid. Mis on hemoglobiini nii olulise muutuse põhjus? Ingram eraldas sirprakulise aneemiaga patsientide verest hemoglobiini ja analüüsis selle esmast struktuuri. Samal ajal selgus, et patsientide hemoglobiini ja tervete hemoglobiini erinevus seisneb ainult selles, et 6. kohal (N-otsast) olevate patsientide hemoglobiini polüpeptiidahelas on valiini jääk (val), samas kui terve hemoglobiin sisaldab glutaalhapet (glu). Hemoglobiini molekul koosneb neljast alaühikust (neli polüpeptiidahelat_ - kaks alfa- ja kaks beeta-ahelat, mille aminohappejääkide koguarv on: 141?2 + 146?2 + 574. Toimub "glu" asendamine "val"-ga alfa-ahelates, st kahes ahelas neljast. Seega piisab 574 aminohappejäägist koosneva molekuli puhul ainult kahe asendamisest ja ülejäänud 572 muutmata jätmisest, nii et hemoglobiini omadustes tekivad põhjalikud muutused. Kui muudate selle võimet kristalliseeruda ja hapnikku siduda, on sellel inimese tervisele saatuslikud tagajärjed.
Sanger (Cambridge, Inglismaa) alustas insuliinivalgu esmase struktuuri dešifreerimist juba 1940. aastatel. Piinliku ja aeganõudva uurimistöö käigus töötas Sanger välja hulga uusi analüüsimeetodeid ja -võtteid. Neid töid tegi ta enam kui 10 aastat ja neid kroonis täielik edu: loodi insuliini valem ja autor pälvis silmapaistvate saavutuste eest Nobeli preemia (1958). Sangeri töö tähtsus ei seisne mitte ainult insuliini esmase struktuuri lahtimõtestamises, vaid ka selles, et on saadud kogemusi, välja töötatud uusi meetodeid ja nende uuringute reaalsus on tõestatud. Pärast Sangeri tööd oli seda teistel uurijatel lihtsam teha. Tõepoolest, pärast Sangerit alustasid paljud laborid tööd mitmete valkude primaarstruktuuri dešifreerimiseks, täiustasid analüüsimeetodeid ja töötasid välja uusi meetodeid.
VIII. VALGIDE FUNKTSIOONID
katalüütiline
Valgud – ensüüme toodavad elusorganismid; neil on katalüütiline toime, see tähendab võime suurendada teatud keemiliste reaktsioonide kiirust. Ensümaatilisel toimel põhinevad käärimisprotsessid, mida on kasutatud juba eelajaloolistest aegadest veinide, äädika, õlle ja leiva valmistamisel. 1680. aastal kasutas Hollandi loodusteadlane Anthony Leeuwenhoek pärmi- ja bakterirakkude vaatlemiseks enda disainitud mikroskoopi; elusorganismideks ta neid siiski ei pidanud. 1857. aastal näitas Louis Pasteur, et pärm on elusorganism ja käärimine on füsioloogiline protsess. 1897. aastal õnnestus E. Buchneril tõestada, et käärimine võib toimuda ka tervete pärmirakkude osaluseta. Pärast pärmirakkude ekstraheerimist sai ta lahuse, mis ei sisalda rakke, kuid millel on ensümaatiline aktiivsus (sisaldab ensüümi või ensüümi). Sõna "ensüüm" tuleb kreeka sõnast en 2yme – juuretises.
Kuni 1926. aastani ei saadud tõendeid selle kohta, et ensüümid on valgud. Alles 1926. aastal õnnestus Cornelli ülikoolis töötanud James B. Sumneril (1887–1955) isoleerida sojaubadest puhas ureaas ja saada ensüümi ureaasi kristalne vorm, valk, mis katalüüsib uurea hüdrolüütilist lõhustamist.
CO(NH2)2 + H2O - CO2 + 2NH3
Ureaasi molekulmass on 480 000; molekul koosneb kuuest subühikust.
Tuntud on umbes 2000 erinevat ensüümi, mõnda neist on üksikasjalikult uuritud. Kaasaegse klassifikatsiooni järgi on kõik ensüümid jagatud kuueks klassiks.
1. Oksireduktaasid ehk redoksensüümid. seda suur grupp, mis koosneb 180-190 ensüümist. Oksireduktaasid kiirendavad erinevate kemikaalide oksüdeerumist või redutseerimist. Seega katalüüsib sellesse klassi kuuluv ensüüm alkoholdehüdrogenaas etüülalkoholi oksüdeerumist atseetaldehüüdiks ja mängib olulist rolli alkohoolse kääritamise protsessis.
Ensüüm lipoksügenaas oksüdeerib õhuhapnikuga küllastumata rasvhappeid. Selle ensüümi toime on üks jahu ja teravilja rääsumise põhjusi.
2. Transferaasid. Selle ensüümide rühma esindajad katalüüsivad erinevate rühmade üleminekut ühest molekulist teise, näiteks ensüüm türosiinaminotransferaas katalüüsib aminorühma ülekandmist. Selle rühma ensüümid mängivad meditsiinis olulist rolli.
3. Hüdrolaasid. Selle rühma ensüümid katalüüsivad hüdrolüüsireaktsioone. Selle ensüümide rühma esindajatel on suur tähtsus seedimisprotsessides, toiduainetööstuses ja muudes tööstusharudes. Niisiis, ensüüm lipaas katalüüsib glütseriidide hüdrolüüsi vabade rasvhapete ja glütserooli moodustumisega. Pektiinainete hüdrolüüs toimub pektolüütiliste ensüümide osalusel, nende kasutamine võimaldab suurendada saaki ning selgitada puuvilja- ja marjamahla.
Hüdrolaaside rühm on amülaasid, mis katalüüsivad tärklise hüdrolüüsi. Nad on leidnud laialdast rakendust alkoholi-, pagari-, tärklise- ja siirupitööstuses.
Hüdrolaasid hõlmavad suurt hulka proteolüütilisi ensüüme, mis katalüüsivad valkude ja peptiidide hüdrolüüsi. Neid kasutatakse kerges ja toiduainetööstuses. Nende abiga transpordivad nad liha, naha "pehmenemist", juustu saamist.
4. Lüaasid. Katalüüsige lõhustamisreaktsioone süsinikuaatomite, süsiniku ja hapniku, süsiniku ja lämmastiku, süsiniku ja halogeeni vahel. Selle rühma ensüümide hulka kuuluvad dekarboksülaasid, mis eraldavad süsinikdioksiidi molekuli orgaanilistest hapetest.
jne.................